 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用pH玻璃电极为指示电极,以0.200 0 mol.L -3NaOH溶液滴定0.020 00 mol.L-1苯甲酸溶液。从滴定曲线
A.6.0×10-9
B.6.6×10-5
C.6.6×10-9
D.数据少无法确定
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.6.0×10-9
B.6.6×10-5
C.6.6×10-9
D.数据少无法确定
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“用pH玻璃电极为指示电极,以0.200 0 mol.L -3…”相关的问题
更多“用pH玻璃电极为指示电极,以0.200 0 mol.L -3…”相关的问题
A.6.0×10-9;
B.6.6×10-5;
C.6.6×10-9;
D.数据少无法确定。
用玻璃电极作指示电极,以0.200mol·L-1苯甲酸溶液,从滴定曲线上求得终点时溶液的pH为8.22,二分之一终点时溶液pH为4.18,试计算苯甲酸的解离常数。
用c[La(NO3)3]=0.03318mol·L-1La(NO3)3溶液滴定100·0mL0.03095mol·L-1的NaF溶液,滴定反应为:La3++3F-====LaF3↓。用固体LaF3膜电极为指示电极(正极),饱和甘汞电极为参比电极(负极),测得其滴定数据如下:
| V[La(NO3)3]/mL | 电池电动势E/V |
| 0.00 30.30 30.60 30.90 31.20 31.50 32.50 50.00 | -0.1046 0.0041 0.0179 0.0410 0.0656 0.0769 0.0888 0.1118 |

在pH=3.0,Cu2+浓度为0.20mol/L的缓冲溶液中,以铂作为阳极沉积铜,此时O2在铂电极上生成,且分压为1.00atm,电池的电阻是2.80Ω,温度是25℃,铜极为阴极。求:(1)铜开始析出的理论分解电压是多少;(2)当电流为0.15A时,iR降是多少;(3)若氧的过电位是0.85V,那么分解电压是多少;(4)若Cu2+浓度为0.001mol/L,其他条件都不变,其分解电压是多少。
用CLa(No3)3=0.03318mol?L-1的La(NO3)3溶液滴定100.0mL 0.03095mol?L-1的NaF的溶液,滴定反应为:
 ,用固体LaF。膜电极为指示电极(正极),饱和甘汞电极为参比电极(负级),测得其滴定数据为:
,用固体LaF。膜电极为指示电极(正极),饱和甘汞电极为参比电极(负级),测得其滴定数据为:
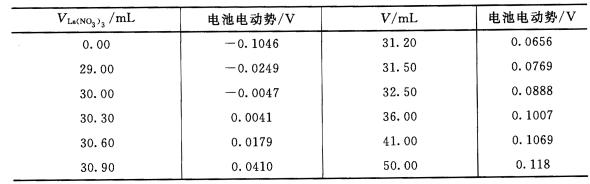 (1)计算反应完全时所需滴定剂的体积,并将其与电位滴定确定终点时消耗滴定剂的体积相比较。 (2)已知电池电动势与F一浓度的关系为:E=K+0.0592PF,用所测第一组数据算出K值。 (3)用求得的K值,计算加入50.00mI.,滴定剂后r的浓度?(设活度系数不变)
(1)计算反应完全时所需滴定剂的体积,并将其与电位滴定确定终点时消耗滴定剂的体积相比较。 (2)已知电池电动势与F一浓度的关系为:E=K+0.0592PF,用所测第一组数据算出K值。 (3)用求得的K值,计算加入50.00mI.,滴定剂后r的浓度?(设活度系数不变)
当下列电池中的标准溶液是pH=5.21的缓冲溶液时,在25℃时的电动势为0.209V。
玻璃电极|H+(a)||SCE。
当缓冲溶液由待测试液代替时,测得的电动势为0.312V,计算待测试液的pH。