 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
凡是中心原子采取sp3d2杂化轨道成键的分子,其空间构型为( )。
A.八面体
B.平面四方形
C.四方锥
D.以上三种都有可能
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.八面体
B.平面四方形
C.四方锥
D.以上三种都有可能
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“凡是中心原子采取sp3d2杂化轨道成键的分子,其空间构型为(…”相关的问题
更多“凡是中心原子采取sp3d2杂化轨道成键的分子,其空间构型为(…”相关的问题
判断下列分子的几何构型、键角、中心原子的杂化轨道类型,并判断分子的极性。
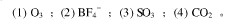
实验测定:Mn(Py)2Cl2(Py为吡啶分子)的磁矩为3.88μB,试指出:
中心原子氧化态______;中心原子的配位数______;
中心原子的单电子数______;配合物的空间几何构型______;
中心原子的杂化轨道类型______。
已知一些铂金属配合物,如cis-PtCl4(NH3)2,cis-PtCl2(NH3)2和cis-PtCl2(en)可以作为活性抗癌剂(所有反式异构体均无抗癌活性),实验测得它们都是抗磁性物质。试用价键理论画出这些配合物的杂化轨道图,它们是内轨型配合物还是外轨型配合物?各采用哪种类型的杂化轨道成键?
填写下列表格:
| 分子 | IF3 | IF5 | IF7 |
| 中心原子价层电子对数 | |||
| 中心原子价层电子对几何构型 | |||
| 分子空间几何构型 | |||
| 中心原子杂化轨道类型 (注明等性或不等性) | |||
根据价层电子对互斥理论,填写下表:
| 分子 | SO3(g) | SCl2(g) | XeF2 |
| 中心原子价层电子对数 | |||
| 中心原子价层电子对几何构型 | |||
| 分子空间几何构型 | |||
| 中心原子杂化轨道类型 (注明等性或不等性) | |||
| 分子有无极性 | |||
| 分子间作用力 |
根据配合物的价键理论,指出下列配离子其中心离子的电子排布、杂化轨道的类型和配离子的空间构型。
[Mn(H2O)6]2+[Ag(CN)2] [Cd(NH3)4]2+[Ni(CN)4]2-[Co(NH3)6]3+
下列化合物中中心原子采用sp3杂化方式的是( )。
(A) H2O (B) CCl4(C) NH3(D) 以上都是
下列分子或离子中,中心原子各采用哪种杂化方式?
NCl3,SF4,CHCl3,H3O+, IF3
IF3
实验测得[Co(NH3)6]3+配离子是抗磁性的,试问:
(1)它的空间构型是什么?根据价键理论Co3+采用什么样的杂化轨道与配位体NH3分子形成配位健?
(2)根据晶体场理论绘出此配离子两种可能的d电子构型,表明它们的高低自旋和磁性情况,对此配离子哪种情况是正确的?
(3)当[Co(NH3)6]3+被还原为[Co(NH3)6]2+时,磁矩约为4~5B.M.,绘出其可能的d电子构型,说明它们的磁性情况。
配合物K3[Fe(CN)5(CO)]中配离子的电荷数应为______,配离子的空间构型为______,配位原子为______,中心离子的配位数为______。中心离子所采取的轨道杂化方式为______,该配合物属______磁性分子。