 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
PbI2和CaCO3的溶度积均近似为10-9,因此两者的饱和溶液中Pb2+的浓度近似与Ca2+的浓度相等。()
PbI2和CaCO3的溶度积均近似为10-9,因此两者的饱和溶液中Pb2+的浓度近似与Ca2+的浓度相等。( )
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
PbI2和CaCO3的溶度积均近似为10-9,因此两者的饱和溶液中Pb2+的浓度近似与Ca2+的浓度相等。( )
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“PbI2和CaCO3的溶度积均近似为10-9,因此两者的饱和…”相关的问题
更多“PbI2和CaCO3的溶度积均近似为10-9,因此两者的饱和…”相关的问题
A.1.2 × 10-12 ;
B. 6.2 × 10-6 ;
C. 4.8 × 10-7 ;
D. 2.9 × 10-15
某学生为测定CuS的溶度积常数,设计如下原电池:正极为铜片,在0.1mol·dm-3Cu2+的溶液中,再通入H2S气体使之达到饱和;负极为标准锌电极。测得电池电动势为0.670V。已知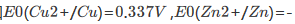 0.763V,H2S的
0.763V,H2S的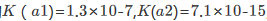 。试求CuS的溶度积常数。
。试求CuS的溶度积常数。
在25℃时测得碘酸铜饱和溶液的电导率为6.28×10-4S·cm-1,Cu2+和IO3-的摩尔电导率分别为55和41 S·cm2·mol-1。所用水的电导率小于1μs·cm-1,可以忽略不计。试求Cu(IO3)2的溶度积常数是多少?
A.Cl-及I-以相同量沉淀
B.Cl-沉淀量更多
C.I-沉淀量更多
D.I-比Cl-沉淀略多一些
A.2304
B.2360
C.2344
D.1320
已知25℃时AgBr(s)的溶度积Ksp=6.3×10-13。利用表7.3.2(在教材中)中的数据计算25℃时用绝对纯的水配制AgBr饱和水溶液的电导率,计算时要考虑水的电导率。
已知25℃时AgBr的溶度积Ksp=4.88×10-13,EΘ(Ag+/Ag)=0.7994V,EΘ(Br2/Br-)=1.065V,试计算25℃时:(1)银-溴化银电极的标准电极电势EΘ(AgBr(s)/Ag);(2)AgBr(S)的标准生成吉布斯函数。
以CaCO3为基准物标定EDTA(pH=10),若配制EDTA的水中含有Ca2+,用标定后的EDTA滴定Pb2+,以二甲酚橙为指示剂(pH=6),测定Pb2+结果______。(指偏高、低或无影响)
已知
