 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
将反应H++OH-====H2O设计成可逆电池,选出下列电池中正确的一个。( )
A.Pt|H2|H+(aq)||OH-(aq)|O2|Pt
B.Pt|H2|NaOH(aq)|O2|Pt
C.Pt|H2|NaOH(aq)||HCl(aq)|H2|Pt
D.Pt|H2(p1)|H2O(l)|H2(p2)|Pt
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.Pt|H2|H+(aq)||OH-(aq)|O2|Pt
B.Pt|H2|NaOH(aq)|O2|Pt
C.Pt|H2|NaOH(aq)||HCl(aq)|H2|Pt
D.Pt|H2(p1)|H2O(l)|H2(p2)|Pt
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“将反应H++OH-====H2O设计成可逆电池,选出下列电池…”相关的问题
更多“将反应H++OH-====H2O设计成可逆电池,选出下列电池…”相关的问题
将反应2Cu(s)+HgO(s)→Hg(l)+Cu2O(s)设计成电池时,其电池表示为______。
将反应Ag(s)→Ag-Au(合金,a(Ag)=0.1)设计成原电池图式为______,25℃时该电池的电动势E=______。
298K时,反应H2(g)+Ag2O(s)====2Ag(s)+H2O(l)的恒容热效应QV=-252.79kJ·mol-1。在298K、标准压力下,将上述反应体系构成一可逆原电池,则其电动势的温度系数为-5.044×10-4V·K-1。求Ag(s)|Ag2O(s)|OH-电极的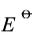 。已知298K时水的离子积Kw=1×10-14。
。已知298K时水的离子积Kw=1×10-14。
 ,H2O(l)的饱和蒸气压为2.33kPa,则( )。
,H2O(l)的饱和蒸气压为2.33kPa,则( )。A.因 ,故20℃时H2O(g)将全部变为液态
,故20℃时H2O(g)将全部变为液态
B.因20℃时 ,故此温度下,H2O(l)和H2O(g)不能达到平衡
,故此温度下,H2O(l)和H2O(g)不能达到平衡
C.在20℃,p(H2O)=2.33kPa时,此过程
D.20℃,水蒸气压为 时,平衡向形成H2O(g)的方向移动
时,平衡向形成H2O(g)的方向移动
据报道,美国化学家研究出一种催化剂,用它在常温常压下可用水与氮气制得氨。可能是下列反应吗?为什么?
N2(g)+H2O(1)→NH3(g)+O2(g)
{已知:298.15K时,H2O(l)、NH3(g)的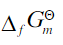 分别为-237.2kJ·mol-1和-16.5kJ·mol-1}
分别为-237.2kJ·mol-1和-16.5kJ·mol-1}
CO2(g)与H2S(g)在高温的反应为CO2(g)+H2S(g)===COS(g)+H2O(g),今在610K时将4.4g的CO2(g)加入体积为2.5dm3的空瓶中,然后再充入H2S(g)使总压为1000kPa。达平衡后取样分析,得其中H2O(g)的摩尔分数为0.02。将温度升至620K重复上述实验,达平衡后取样分析. 得其中H2O(g)的摩尔分数为0.03。视气体为理想气体,试计算:
(1)610K时的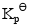 ;
;
(2)610K时的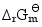 ;
;
(3)反应的标准摩尔焓变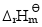 (设其不随温度而变);
(设其不随温度而变);
(4)610K时,往该体积的瓶中充入不参与反应的气体,直至压力加倍,则COS(g)的产量有何变化。若充入不参与反应的气体,保持压力不变,而使体积加倍,COS(g)的产量又有何变化。
将1mol H2O(g)从373K、100kPa下,小心等温压缩,在没有灰尘等凝聚中心时,得到了373K、200kPa的介稳水蒸气,但不久介稳水蒸气全变成液态水,即
H2O(g,373K,200kPa)===H2O(l,373K,200kPa)
求该过程的△H、△G和△S。已知在该条件下,水的摩尔汽化热为46.02kJ·mol-1,水的密度为1000kg·m-3。设气体为理想气体,液体体积受压力的影响可忽略不计。
在298K反应BaCl2·H2O(s)====BaCl2(s)+H2O(g)达平衡时,p(H2O)=330Pa。则反应的ΔrGθm为( )kJ·molq-1。
(A) -14.2 (B) 14.2 (C) 142 (D) -142