 更多“一封闭系统的任一可逆变化途径都可在其状态图上表现为实线。”相关的问题
更多“一封闭系统的任一可逆变化途径都可在其状态图上表现为实线。”相关的问题
A.不作非体积功条件下,QV与途径无关,故QV是状态函数;
B.不作非体积功条件下,Qp与途径无关,故Qp是状态函数;
C.系统发生一确定变化,不同途径中,热肯定不相等;
D.系统发生一确定变化,则Q+W与途径无关。
。画出p-V示意图,并把△U和W,值按大小次序排列。
(1)等温可逆膨胀;
(2)绝热可逆膨胀;
(3)沿着p/Pa=1.0×104Vm/(dm3·mol-1)+b的途径可逆变化。
始态为T1=300K,P1=200kPa的某双原子理想气体1mol,经下列不同途径变化到T2=300K,P2=100kPa的末态。求各步骤及途径的Q,△S。
(1)恒温可逆膨胀;(2)先恒容冷却至使压力降至100kPa,再恒压加热至T2;(3)先绝热可逆膨胀到使压力降至100kPa,再恒压加热至T2。
下述说法是否正确:(1)不可逆过程的熵变△s无法计算;(2)如果从同一初始态到同一终态有两条途径,一为可逆,另一为不可逆,则△S不可逆>△S可逆,Sf,不可逆>Sf,可逆,Sf,不可逆>Sf,可逆;(3)不可逆绝热膨胀终态熵大于初态熵S2>S1,不可逆绝热压缩终态熵小于初态熵S2<S1;(4)工质经过不可逆循环∮ds>0,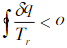 。
。
1mol单原子理想气体,由温度为273K,体积为22.4dm3的始态,经由Ⅰ途径变化到温度为546K、体积仍为22.4dm3;再经由Ⅱ途径定温可逆膨胀至体积为44.8dm3;最后经由Ⅲ途径使系统定压回到其初态。试求出:
(1) 各状态下的气体压力;
(2) 系统经由各途径时的Q,W,△U,△H;
(3) 该循环过程的Q,W,△U,△H。
求证在理想气体p-V图上任一点处,绝热可逆线的斜率的绝对值大于恒温可逆线的斜率的绝对值。

A.q<0,ω>0,△u<0
B.q>0,ω<0,Δu>0
C.q<0,ω>0,△u>0
D.q>0,ω>0,△u<0
CSTR的稳定操作状态
在一全混流反应釜中进行下述一级不可逆液相反应:
k1=1.8×106exp(-6039.25/T),反应混合物的密度ρ和比热cp,均为常数,ρ=1.2g/cm3,cP=3.768J/(g·K)。在20℃液料以200cm3/s的速度进入反应釜。原料中只含反应物A,其初浓度为4mol/L。反应釜的体积为10L。反应在绝热条件下进行。已知该反应的热效应为△Hr=-192.95kJ/mol。试确定该反应体系的稳定工作点和相应的转化率。
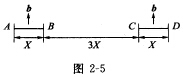
有两个被钉扎住的刃型位错AB和CD,它们的长度x相等,且具有相同的b,而b的大小和方向相同(图2-5)。每个位错都可看做F-R位错源。试分析在其增殖过程中二者间的交互作用。若能形成一个大的位错源,使其开动的τc需多大?若两位错b相反,情况又如何?


 如果结果不匹配,请
如果结果不匹配,请 


















