 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
PCl5加热分解为PCl3和Cl2,将2.695g PCl5装入1L容器中,在250℃时达到平衡后,总压力为101.325kPa,求PCl5的分解
PCl5加热分解为PCl3和Cl2,将2.695g PCl5装入1L容器中,在250℃时达到平衡后,总压力为101.325kPa,求PCl5的分解率及分解反应的K。(PCl5的分子量为208.22)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
PCl5加热分解为PCl3和Cl2,将2.695g PCl5装入1L容器中,在250℃时达到平衡后,总压力为101.325kPa,求PCl5的分解率及分解反应的K。(PCl5的分子量为208.22)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“PCl5加热分解为PCl3和Cl2,将2.695g PCl5…”相关的问题
更多“PCl5加热分解为PCl3和Cl2,将2.695g PCl5…”相关的问题
PCl5的分解反应为PCl5(g)==PCl3(g)+Cl2(g),在523K、100kPa下达成平衡,测得平衡混合物的密度ρ=2.695kg.m-3。试计算:(1)PCl5(g)的解离度;(2)该反应的 和
和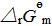 。
。
五氯化磷分解反应为PCl5(g)===PCl3(g)+Cl2(g)。在200℃时的KΘ=0.312,计算:(1)200℃,200kPa下PCl5的解离度;(2)摩尔比为1:5的PCl5与Cl2的混合物,在200 oc,101.325 kPa下,达到化学平衡时PCI5的解离度。
在一定温度和压强下,某一定量的PCl5气体的体积为1dm3,此时PCl5气体已有50%解离为PCl3和Cl2气体。试判断在下列条件下,PCl5的解离度是增大还是减小。
(1) 减压使PCl5的体积变为2dm3;
(2) 保持压强不变,加入氮气使体积增至2dm3;
(3) 保持体积不变,加入氮气使压强增加1倍;
(4) 保持压强不变,加入氯气体积变为2dm3;
(5) 保持体积不变,加入氯气使压强增加1倍。
某温度下,反应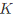 的平衡常数
的平衡常数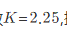 。把一定量的PCl5引入一真空瓶内,达平衡后PCl5的分压为2.533×104Pa,则PCl3的分压是______Pa,PCl5的解离分数______。
。把一定量的PCl5引入一真空瓶内,达平衡后PCl5的分压为2.533×104Pa,则PCl3的分压是______Pa,PCl5的解离分数______。
在375K时反应SO2Cl2(g)=SO2(g)+Cl2(g)的标准平衡常数Kθ为2.4。今将5.4g的SO2Cl2(g)置于密闭容器中,并加热到375K。(1) 假定SO2Cl2(g)不解离,它的压力将是多少?(2) 平衡时SO2Cl2(g)、SO2(g)和Cl2(g)的分压各是多少?
设在某一温度下,有一定量的PCl5(g)在100kPa压力下的体积为1dm3,在该条件下PCl5(g)的解离度α=0.5。用计算说明在下列几种情况下,PCl5(g)的解离度是增大还是减小。
(1)使气体的总压降低,直到体积增加到2dm3;
(2)通入N2(g),使体积增加到2dm3,而压力仍为100kPa;
(3)通入N2(g),使压力增加到200kPa,而体积仍维持为1dm3;
(4)通入Cl2(g),使压力增加到200kPa,而体积仍维持为1dm3。
给出下列物质的水解反应方程式,并说明NCl3水解产物与其他化合物的水解产物有何本质的区别?为什么?
(1) NCl3;
(2) PCl3;
(3) AsCl3;
(4) SbCl3;
(5) BiCl3;
(6) POCl3。
氢气和氯气化合形成氯化氢的反应:H2(g)+Cl2(g)→2HCl(g),根据下列反应机制推导其速率方程:
(1) (快速平衡)
(快速平衡)
(2)Cl+H2→HCl+H (慢)
(3)H+Cl2→HCl+Cl (快)
将2500kg·h-1NaOH水溶液在一单效蒸发器内从10%(质量分数,下同)蒸发浓缩到25%。已知加热蒸汽的绝对压力为450kPa,蒸发室内的压力为101.33kPa,溶液的沸点为115℃,比定压热容为3.9kJ·kg-1·℃-1,热损失为20kW。试计算:
(1) 进料温度为20℃时,所需加热蒸汽消耗量和单位蒸汽消耗量;
(2) 沸点进料时,所需加热蒸汽消耗量和单位蒸汽消耗量。
在战略实施中,将经营战略分解为几个战略实施阶段的做法是()。
A.战略发动
B.战略计划
C.战略运作
D.战略分析