 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
浓度均为0.0100mol·L-1的Zn2+、Cd2+混合溶液,加入过量KI,使终点时游离I-浓度为1mol·L-1,在pH=5.0时,以二甲酚浓度均为0.0100mol·L-1的Zn2+、Cd2+混合溶液,加入过量KI,使终点时游离I-浓度为1mol·L-1,在pH=5.0时,以二甲酚橙(XO)为指示剂,用等浓度的EDTA滴定其中的Zn2+,计算终点误差。(lgKZnY=16.50,lgKCdY=16.46;pH=5.0时,lgαY(H)=6.45、lgK'Zn-XO=4.8;Cd2+-I-络合物的Igβ1~lgβ4分别为2.10、3.43、4.49、5.41)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“浓度均为0.0100mol·L-1的Zn2+、Cd2+混合溶…”相关的问题
更多“浓度均为0.0100mol·L-1的Zn2+、Cd2+混合溶…”相关的问题
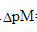 =0.2 mol·L-1,判断能否准确滴定。达化学计量点时,未络合的Zn2+百分数是多少?(pH=10.0时,αZn(OH)=102.4,lgαY(H)=0.5,lgKZnY=16.50,锌氨络合物的lgβ1~lgβ4分别为2.27、4.61、7.01、9.06
=0.2 mol·L-1,判断能否准确滴定。达化学计量点时,未络合的Zn2+百分数是多少?(pH=10.0时,αZn(OH)=102.4,lgαY(H)=0.5,lgKZnY=16.50,锌氨络合物的lgβ1~lgβ4分别为2.27、4.61、7.01、9.06 (Ag2CrO4)=1.1×10-12,
(Ag2CrO4)=1.1×10-12, (BaCrO4)=1.2×10-10,
(BaCrO4)=1.2×10-10, (PbCrO4)=1.8×10-14
(PbCrO4)=1.8×10-14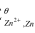 (zn2+/zn)=-0.763V)
(zn2+/zn)=-0.763V) (Cu2+/CuCl)和
(Cu2+/CuCl)和 =8.4×10-4,0.10mol·L-1此酸的c(H+)浓度为( )
=8.4×10-4,0.10mol·L-1此酸的c(H+)浓度为( )
















