 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在0.10mol·dm-3 CdCl2溶液中含有0.30mol·dm-3 HCl,通入H2S至饱和,达到平衡时 (1) H+浓度多大? (2) 留在
在0.10mol·dm-3CdCl2溶液中含有0.30mol·dm-3HCl,通入H2S至饱和,达到平衡时
(1) H+浓度多大?
(2) 留在溶液中的Cd2+浓度多大?
已知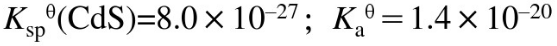 。
。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在0.10mol·dm-3CdCl2溶液中含有0.30mol·dm-3HCl,通入H2S至饱和,达到平衡时
(1) H+浓度多大?
(2) 留在溶液中的Cd2+浓度多大?
已知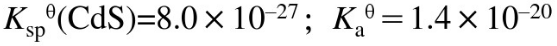 。
。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在0.10mol·dm-3 CdCl2溶液中含有0.30mo…”相关的问题
更多“在0.10mol·dm-3 CdCl2溶液中含有0.30mo…”相关的问题
将0.050dm3,浓度为0.10mol·dm-3一元弱酸HA溶液与0.020dm3,0.10mol·dm-3KOH溶液混合后稀释至0.10dm3,测得溶液pH=5.25,求HA的解离常数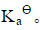 。
。
试用近似计算说明,在0.10mol·dm-3的HAc溶液中通入H2S达饱和(约0.1mol·dm-3H2S),能否使溶液中0.10mol·dm-3的Mn2+以MnS形式沉淀出来?(已知K(HAc)=1.8×10-5,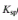 (MnS)=1.4×10-15,H2S的K1=1.32×10-7,K2=7.10×10-15)
(MnS)=1.4×10-15,H2S的K1=1.32×10-7,K2=7.10×10-15)
在0.10mol·dm-3HAc溶液中加入少许NaCl晶体,溶液的pH将会______;若以Na2CO3代替NaCl,则溶液的pH将会______。
已知H2CO3的

150cm30.10mol·dm-3HAc溶液和50cm30.10mol·dm-3NaOH溶液混合,若已知HAc的的解离常数Ka=1.8×10-5,试求混合溶液的[H+]。
根据书(教材)末附录6和附录7的数据(不进行具体计算),将下列化合物的0.10mol·dm-3溶液按pH值增大的顺序排列之。
(1)HAc (2)NaAc (3)H2SO4(4)NH3(5)NH4Cl (6)NH4Ac
由两个氢电极H2(100kPa)|H+(0.10mol·dm-3)|Pt和H2(100kPa)|H+(xmol·dm-3)|Pt组成原电池,测得该原电池的电动势为0.016V。若后一电极作为该原电池的正极,求组成该电极的溶液中H+的浓度x的值。
已知氨水的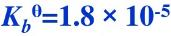 ,现有1.0dm30.10mol·dm-3氨水,试求:
,现有1.0dm30.10mol·dm-3氨水,试求:
(1) 氨水的[H+]。
(2) 加入10.7g NH4Cl后,溶液的[H+](加入NH4Cl后溶液体积的变化忽略不计)。
(3) 加入NH4Cl后,氨水的解离度缩小的倍数。
A.8.7
B.7.0
C.7.8
D.9.0
某难溶电解质A3B2在水中的溶解度s=1.0×10-6mol·dm-3,则在其饱和溶液中c(A2+)=______,c(B3-)=______,