 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
试用气体动理论说明,一定体积的氢和氧的混合气体的总压强等于氢气和氧气单独存在于该体积内时所产生的压强
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“试用气体动理论说明,一定体积的氢和氧的混合气体的总压强等于氢…”相关的问题
更多“试用气体动理论说明,一定体积的氢和氧的混合气体的总压强等于氢…”相关的问题
两容器分别贮有气体A和B,温度和体积都相同,试说明在下列各种情况中它们的分子的速度分布是否相同:(1)A为氮,B为氢,而且氮和氢的质量相等,即mA=mB;(2)A和B均为氢气,但mA≠mB;(3)A和B均为氢气,而且mA=mB,但是使A的体积等温地膨胀到原体积的二倍.
试用分子轨道理论解释Na2O2中的O2-(过氧离子)是逆磁性的而KO2中的O2-(超氧离子)是顺磁性的,并计算相应的磁矩。
348K时,0.3kgNH3(g)的压力为1.61×103kPa,试用下述两种方法计算其体积。试比较哪种方法计算出来的体积与实测值更接近(已知实测值为28.5dm3)。已知在该条件下NH3(g)的临界参数为Tc=405.6K,pc=1.13×104kPa;van der Waals气体常数为a=0.417Pa·m6·mol-2,b=3.71×10-5m3·mol-1。(1)用van der Waals气体状态方程式;(2)用压缩因子图。
试用杂化轨道理论说明PCl3(键角101°)分子的中心原子所采用的杂化轨道类型及其成键情况。
大气中含CO2约0.031%(体积分数),试用化学热力学分析说明,菱镁矿(Mg-CO3)能否稳定存在于自然界?已知相关热力学数据如下:
MgCO3(s)→MgO(s)+CO2(g)
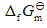 (298.15K)/kJ·mol-1-1012.1 -569.3 -394.4
(298.15K)/kJ·mol-1-1012.1 -569.3 -394.4
在索末菲模型中,证明有N个电子的金属中,自由电子气体在绝对零度时的动能为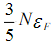 ;由此导出压强P和体积弹性模量
;由此导出压强P和体积弹性模量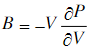 的表达式。求出锂(体心立方结构.品格常数为3.5
的表达式。求出锂(体心立方结构.品格常数为3.5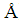 )的体积弹性模量值,并与杨氏模量的量级1011N/m2比较。
)的体积弹性模量值,并与杨氏模量的量级1011N/m2比较。
在一定的温度和压力下,两种不同的气体具有相同的体积,则这两种气体的( )。
(A) 分子数相同 (B) 相对分子质量相同
(C) 质量相同 (D) 密度相同
1mol氢,在压强为1.0×105Pa、温度为20℃时,其体积为V0.今使它经以下两个过程达到同一状态:(1)先保持体积不变,加热使其温度升高到80℃,然后令它等温膨胀,体积变为原来的2倍;
(2)先使它等温膨胀至原体积的2倍,然后保持体积不变,加热到80℃.
试分别计算以上两种过程中吸收的热量,气体对外作的功和内能的增量;并作出p-V图.
在索末菲模型中,证明有N个电子的金属中,自由电子气体在绝对零度时的动能为

 )的体积弹性模量值,并与杨氏模量的量级1011N/m2比较。
)的体积弹性模量值,并与杨氏模量的量级1011N/m2比较。
1mol氢,在压强为1.0×105Pa,温度为20℃时,其体积为V0。今使它经以下两种过程达同一状态:(1)先保持体积不变,加热使其温度升高到80℃,然后令它作等温膨胀,体积变为原体积的2倍;(2)先使它作等温膨胀至原体积的2倍,然后保持体积不变,加热到80℃。试分别计算以上两种过程中吸收的热量、气体对外做的功和内能的增量;并作出p-V图。