 更多“用外推法测定电解质溶液无限稀释时摩尔电导率的方法只适用于__…”相关的问题
更多“用外推法测定电解质溶液无限稀释时摩尔电导率的方法只适用于__…”相关的问题
已知25℃时0.01mol·dm-3KCl溶液的电导率为0.141S·m-1,一电导池中充以此溶液,在25℃时测知其电阻为484Ω。在同一电导池中盛入同样体积的浓度分别为0.0005mol·dm-3、0.0010mol·dm-3、0.0020mol·dm-3和0.0050mol·dm-3的NaCl溶液,测出其电阻分别为10910、5494、2772和1128.9Ω。试用外推法求无限稀释时NaCl的摩尔电导率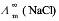 。
。
298K时,某一电导池充满0.01mol/L的KCl溶液(电导率为0.1411S/m)时,测得其电阻为163Ω。若用同一电导池充满0.01mol/L的NH3.H2O时,测得溶液的电阻为2017Ω。试求该NH3.H2O溶液的电离度和电离平衡常数。(已知该温度下,NH4+和OH-的无限稀释摩尔电导率分别为73.4×10-4S.m2/mol和1.98×10-2S.m2/mol。)
用同一电导池分别测定浓度为0.01mol·kg-1、0.1mol·kg-1的两个电解质溶液,如其电阻分别为1000Ω和500Ω,则它们依次的摩尔电导率之比为
(A) 1:5 (B) 5:1 (C) 10:5 (D) 5:10
298K时,已知NaOH、NaCl和NH4Cl溶液无限稀释时的摩尔电导率分别为248.41×10-4S·m2/mol、126.4×10-4S·m2/mol和149.8×10-4S·m2/mol,试计算该温度下NH3·H2O溶液的无限稀释摩尔电导率。
291K时,已知KCl和NaCl的无限稀释摩尔电导率分别为Λm∞ (KCl)=1.2965 ×10-2 S·m2·mol-1 和Λm∞ (NaCl)=1.0860×10-2 S·m2·mol-1,K+和Na+的迁移数分别为t(K+)=0.496,t(Na+)=0.397,试求 在291 K和无限稀释时:
(1)KCl溶液中K+和C1-的离子摩尔电导率;
(2) NaCl溶液中Na+和C1-的离子摩尔电导率。
303K时用稀释黏度计测定了聚苯乙烯-苯溶液(浓度c0=5.5kg/m3)的流出时间数据如下表。(1)试用外推法和一点法计算特性黏数[η];(2)求出Huggins式和Mead-Fuoss式中的斜率系数k'和β值,从而说明此高分子溶液特征;(3)若已知Mark-Houwink方程中的两参数K=0.99×10-2和a=0.73,求此试样的平均相对分子质量。
试液 | 纯溶剂 | 10mL试液 | +5mL苯 | +5mL苯 | +10mL苯 | +10mL苯 |
流出时间/s | 106.8 | 241.6 | 189.7 | 166.0 | 144.4 | 134.2 |
已知25℃时,NaAc,HCl和NaCl无限稀释摩尔电导率分别是91S·cm2·mol-1,426S·cm2·mol-1和126S·cm2·mol-1,H+无限稀释摩尔电导率是350S·cm2·mol-1。计算Ac-无限稀释离子电迁移率。
A.1.474×10-2S·m2·mol-1
B.2.714×10-2S·m2·mol-1
C.2.947×10-2S·m2·mol-1
D.5.428×10-2S·m2·mol-1
一电导池充以0.0200mol·L-1的KCl溶液,298K时测得其电阻为453Ω。已知298K时0.0200mol·L-1的KCl溶液的电导率为0.002765S·cm-1。在同一电导池中,装入同样体积的浓度为0.555g·L-1的CaCl2溶液,测得电阻为1050Ω,计算:(1)电导池常数;(2)CaCl2溶液的电导率;(3)CaCl2溶液的摩尔电导率。(MCaCl2=111.0g·mol-1)
一粉红色固体的实验式为CoCl3·5NH3·H2O,其溶液也呈粉红色,用AgNO3溶液滴定时迅速生成3molAgCl沉淀。粉红色固体受热失去1molH2O,生成紫色固体,其中NH3:Cl:Co的比例不变。紫色固体溶解后,其溶液的摩尔电导值比粉红色溶液小,试推断(画图)粉红色和紫色两个八面体配合物的结构,并分别给以命名。


 如果结果不匹配,请
如果结果不匹配,请 

















