 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298K时,测定乙酸乙酯皂化反应速率。反应开始时,溶液中酯和碱的浓度都为0.01mol·dm-3,每隔一定时间,用标准
在298K时,测定乙酸乙酯皂化反应速率。反应开始时,溶液中酯和碱的浓度都为0.01mol·dm-3,每隔一定时间,用标准酸溶液滴定其中的碱含量,实验所得结果如下:
| t/min | 3 | 5 | 7 | 10 | 15 | 2l | 25 |
| OH-/(10-3mol·dm-3) | 7.40 | 6.34 | 5.50 | 4.64 | 3.63 | 2.88 | 2.54 |

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“在298K时,测定乙酸乙酯皂化反应速率。反应开始时,溶液中酯…”相关的问题
更多“在298K时,测定乙酸乙酯皂化反应速率。反应开始时,溶液中酯…”相关的问题
 ,已知该反应的速率公式为
,已知该反应的速率公式为
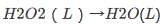
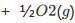 活化能为75kJ·mol-1。当有铁催化剂存在时,该反应的活化能就降低到54kJ·mol-1。计算在298K时此两种反应速率的比值。
活化能为75kJ·mol-1。当有铁催化剂存在时,该反应的活化能就降低到54kJ·mol-1。计算在298K时此两种反应速率的比值。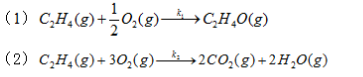

 的
的
















