 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用CaO(s)吸收高炉废气中的SO3气体,其反应方程式为 根据下列数据计算该反应373K时的,以说明反应进行的
用CaO(s)吸收高炉废气中的SO3气体,其反应方程式为
CaO(s)+SO3(g)=CaSO4(s) △H=-401.9KJ/mol
根据下列数据计算该反应373K时的△rGmθ,以说明反应进行的可能性;并计算反应逆转的温度,进一步说明应用此反应防止SO3污染环境的合理性。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用CaO(s)吸收高炉废气中的SO3气体,其反应方程式为
CaO(s)+SO3(g)=CaSO4(s) △H=-401.9KJ/mol
根据下列数据计算该反应373K时的△rGmθ,以说明反应进行的可能性;并计算反应逆转的温度,进一步说明应用此反应防止SO3污染环境的合理性。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“用CaO(s)吸收高炉废气中的SO3气体,其反应方程式为 根…”相关的问题
更多“用CaO(s)吸收高炉废气中的SO3气体,其反应方程式为 根…”相关的问题
计算CaSO4的热分解温度。
CaSO4(s) ==== CaO(s) + SO3(g)
△H/(kJ·mol-1) -1434.1 -635.09 -395.7
△S/(J·K-1·mol-1) 107 39.75 256.6
用一个吸收塔吸收混合废气中的气态污染物A,已知A在气、液两相中的平衡关系为y*=x,气体入口浓度为y1=0.1,液体入口浓度为x2=0.01,
在吸收塔中,用清水自上而下并流吸收混合废气中的氨气。已知气体流量为1000m3/h(标准状态),氨气的摩尔分数为0.01,塔内为常温常压,此条件下氨的相平衡关系为Y*=0.93X,求:
系为y*=x,吸收剂用量为最小用量的1.5倍,气相总传质单元高度为1.2m,要求吸收率为80%,求填料层的高度。
某填料吸收塔高2.7m,在常压下用清水逆流吸收混合气中的氨。混合气入塔的摩尔流率为0.03kmol/(m2·s)。清水的喷淋密度为0.018kmol/(m2·s)。进口气体中的氨体积分数为0.02,已知气相总传质系数Kya=0.1kmol/(m3·s),操作条件下亨利系数为60kPa。试求排出气体中氨的浓度。
将1mol的SO2与1molO2的混合气体,在101.325kPa及903K下通过盛有铂丝的玻璃管,控制气流速度,使反应达到平衡,把产生的气体急剧冷却,并用KOH吸收SO2及SO3。最后量得余下的氧气在101.325kPa,273.15K下体积为13.78dm3,试计算下列反应在903K时的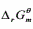 及
及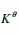 (903K)。
(903K)。
SO2(g)+1/2O2(g)====SO3(g)
用吸收塔吸收废气中的SO2,条件为常压,30℃,相平衡常数为m=26.7,在塔内某一截面上,气相中SO2分压为4.1kPa,液相中SO2浓度为0.05kmol/m3,气相传质系数为kG=1.5×10-5kmol/(m2·h·kPa),液相传质系数为kL=0.39m/h,吸收液密度近似水的密度。试求:

某吸收塔用25mm×25mm的瓷环做填料,充填高度5m,塔径1m,用清水逆流吸收流量为2250m3/h的混合气。混合气中含有丙酮体积分数为5%,塔顶逸出废气含丙酮体积分数降为0.26%,塔底液体中每千克水带有60g丙酮,操作在101.3kPa、25℃下进行,物系的平衡关系为y=2x。试求:
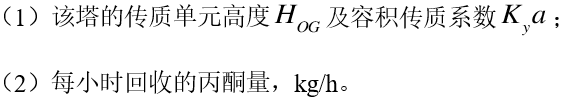
在吸收塔内用清水吸收混合气中的SO2。标准状态下气体流量为5000m3/h,其中S02占5%,要求SO2的嘲收率为95%,气、液逆流接触,在塔的操作条件下,S02在两相问的平衡关系近似为Y*=26.7X,若用水量为最小用水量的1.5倍,用水量应为()。
