 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
理想气体作绝热膨胀,由初状态(p0,V0)至末状态(p,V)。(1)试证明在此过程中气体所做功为;(2)设p0=1.0×106Pa,V0
理想气体作绝热膨胀,由初状态(p0,V0)至末状态(p,V)。(1)试证明在此过程中气体所做功为 ;(2)设p0=1.0×106Pa,V0=0.001m3,p=2.0×105Pa,V=0.00316m3,气体的γ=1.4,试计算气体所做的功。
;(2)设p0=1.0×106Pa,V0=0.001m3,p=2.0×105Pa,V=0.00316m3,气体的γ=1.4,试计算气体所做的功。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
理想气体作绝热膨胀,由初状态(p0,V0)至末状态(p,V)。(1)试证明在此过程中气体所做功为 ;(2)设p0=1.0×106Pa,V0=0.001m3,p=2.0×105Pa,V=0.00316m3,气体的γ=1.4,试计算气体所做的功。
;(2)设p0=1.0×106Pa,V0=0.001m3,p=2.0×105Pa,V=0.00316m3,气体的γ=1.4,试计算气体所做的功。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“理想气体作绝热膨胀,由初状态(p0,V0)至末状态(p,V)…”相关的问题
更多“理想气体作绝热膨胀,由初状态(p0,V0)至末状态(p,V)…”相关的问题
用绝热壁做成一圆柱形的容器,在容器中间放置一无摩擦的、绝热的可动活塞,活塞两侧各有物质的量为ν(以mol为单位)的理想气体.设两侧气体的初始状态均为p0,V0,T0,气体定体摩尔热容CV,m为常量,γ=1.5.将一通电线圈放在活塞左侧气体中,对气体缓慢加热.左侧气体膨胀,同时通过活塞压缩右方气体,最后使右方气体压强增为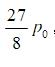 .试问:
.试问:

理想气体从初态1(p1,t1)进行不同过程至相同终压p2,一过程为经过喷管的不可逆绝热膨胀过程,另一过程为经过节流阀的绝热节流过程。若p1>p2>p0,T1>T0(p0,T0为环境压力和温度),试在T-s图上表示此两过程,并根据图比较两过程作功能力损失的大小。
处于环境温度的理想气体由同一初压p1进行不同过程至相同终压p2,一为绝热节流过程,一为定熵膨胀过程。试将绝热节流中损失的作功能力和定熵过程的作功量表示在T-s图中,并比较两者的大小。

一理想气体开始处于T1=300K,p1=3.039×105Pa,V1=4m3。该气体等温地膨胀到体积为16m3,接着经过一等体过程而达到某一压强,从这个压强再经一绝热压缩就能使气体回到它的初态。设全部过程都是可逆的。
4mol某双原子理想气体,由始态600K、1000kPa依次经过下列过程
(1) 绝热反抗600kPa外压膨胀至平衡;
(2) 定容加热至800kPa;
(3) 绝热可逆膨胀至500kPa。
求整个过程的Q,w,△U,△H。
1mol单原子理想气体由始态273K,P经由下列两条途径到达终态T2],p/2:(1) 可逆绝热膨胀;(2) 反抗p/2的恒定外压绝热膨胀。试分别求出两途径的T[2,w,△U,△H,△S和△G;并回答能否由△G来判断过程的方向?已知s(273K)=100J·K-1·mol-1。
273.2K、1MPa、10L的单原子理想气体,绝热膨胀至0.1MPa,计算Q、W、ΔU、△H、△S。(a)pe=p;(b)pe=0.1MPa;(c)pe=0。(单原子分子理想气体)
一定量的理想气体向真空做绝热膨胀,在此过程中气体的()。
A.内能不变,熵减少
B.内能不变,熵增加
C.内能不变,熵不变
D.内能增加,熵增加