 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知298.15K时,,,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的;(4)
已知298.15K时, ,
, ,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的
,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的 ;(4)计算电池反应的
;(4)计算电池反应的 ;(5)求AgI的Ksp。
;(5)求AgI的Ksp。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知298.15K时, ,
, ,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的
,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的 ;(4)计算电池反应的
;(4)计算电池反应的 ;(5)求AgI的Ksp。
;(5)求AgI的Ksp。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知298.15K时,,,标准态时:(1)写出原电池符号(应…”相关的问题
更多“已知298.15K时,,,标准态时:(1)写出原电池符号(应…”相关的问题
已知:
(
H
3
AsO
4
/ H
3
AsO
3
)
=+0.560V
,
(
I
2
/ I
-
)
=+0.5355V
,
F
=96485C
·
mol
-1
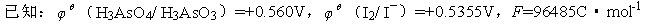
在298.15K时,有下列反应
H3AsO4+2I-+2H+====H3AsO3+I2+H2O

将下列反应组成原电池(温度为298.15K):2Fe3++Cu====2Fe2++Cu2+
(1)计算原电池的标准电动势;(2)写出其电池符号;(3)指出正极、负极,并写出电极反应;(4)当Cu2+的浓度升到10mol·L-1时,原电池的电动势为多少?
8.在298.15K时,有下列反应
H3AsO4+2I-+2H+====H3AsO3+I2+H2O
(1) 计算该反应组成的原电池的标准电动势。
(2) 计算该反应的标准摩尔吉布斯自由能变并指出该反应能否自发进行。
(3) 若溶液的的pH=7,而c(H3AsO4)=c(H3AsO3)=c(I-)=1mol·dm-3此反应的△rGm是多少?此时反应进行方向?
A.当正态总体方差未知时,只能用t分布对总体均值进行估计
B.当正态总体方差已知时,可以用正态分布对总体均值进行估计
C.对于非正态总体,不能用正态分布对总体均值进行估计
D.无论总体分布如何,样本容量比较大时均可以用正态分布对总体均值进行估计
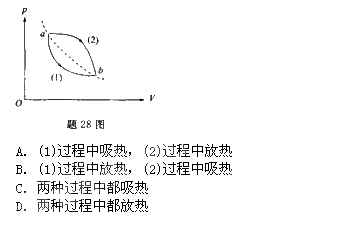
一定量的理想气体,从p-V图上初态a经历(1)或(2)过程到达末态b,已知a、b两态处于同一条绝热线上(图中虚线是绝热线),则气体在()。
某物理体系由两个自旋1/2的非全同粒子组成.已知粒子1处于S1z=1/2的本征态,粒子2处于s2x=1/2的本征态,求体系总自旋S2的可能测值及相应概率.(取h=1)
已知Eθ(MnO-4/Mn2+)=1.51V,Eθ(Cl2/Cl-)=1.36V,若将此两电对组成原电池,请写出:
(1)该电池的电池符号;
(2)写出正负电极的电极反应和电池反应以及电池标准电动势;
(3)计算电池反应在25℃时和Kθ;
(4)当[H+] = 1.0×10-2mol•L-1,而其他离子浓度均为1.0 mol•L-1,= 100 kPa时的电池电动势.
已知某微观体系的力学量A有两个归一一化本征态ψ1、ψ2,相应的本征值为a1、a2.力学量B有两个归一化本征态


当对某个态|ψ〉测量A得到a1后,若再测量B,接着再测A,试求第二次测A得到a1的几率.
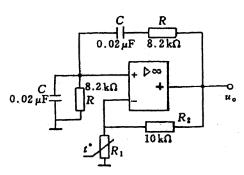
RC振荡电路如图题4.22所示。已知:C=0.02uF,R=8.2kΩ,R2=10kΩ。(1)说明R1应该具有怎样的温度系数和如何选择其冷态电阻;(2)求振荡频率f0。
在RD=SD=“1”时,基本RS触发器()。
(A)置“O”
(B)置“1”
(C)保持原状态
(D)不停地翻转
和齿数分别为:第一对m=4mm,z1=20,z2=40;第二对m'=2mm,z'1=40,z'2=80。若不考虑重合度不同产生的影响,试求在同样工况下工作时,这两款齿轮应力的比值σH/σ'H和σF/σ'F。