 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
含Pb2+、Ca2+的溶液浓度均为2×10-2mol/L。今以同浓度的EDTA分步滴定Pb2+,问:含Pb2+、Ca2+的溶液浓度均为2×10-2mol/L。今以同浓度的EDTA分步滴定Pb2+,问:(1)有无可能分步滴定? (2)滴定适宜酸度范围?(3)选二甲酚橙作指示剂,溶液的最佳酸度是多少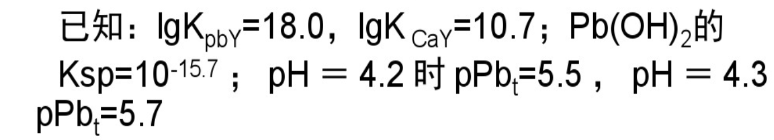
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
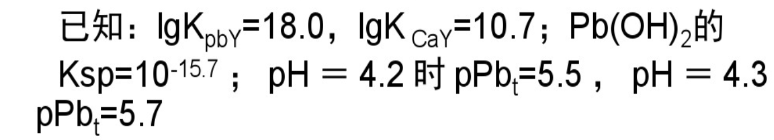
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“含Pb2+、Ca2+的溶液浓度均为2×10-2mol/L。今…”相关的问题
更多“含Pb2+、Ca2+的溶液浓度均为2×10-2mol/L。今…”相关的问题
有一种标准Pb2+溶液,浓度为16.0μg·L-1,显色后测得吸光度为0.250;另含有Pb2+的试液,在同样的条件下显色,测得吸光度为0.320,求(1)试液中Pb2+的浓度;(2)若L=1.0cm,求摩尔吸收系数。[M(Pb)=207g·mol-1]
组成为50%A和50%B的二元混合液,拟用精馏方法将其分离成两种产品。要求塔顶馏出液含99%A,塔釜残液含99%B(均为摩尔分数)。
A和B混合液平衡数据如下所列:
xA | yA |
0.950 | 0.952 |
0.450 | 0.459 |
0.040 | 0.041 |
试求:
(1) 各对浓度下的相对挥发度各为多少?
(2) 最少理论塔板数;
(3) 若原料液组成是70%A和30%B(摩尔分数),产品组成与原题相同,则最少理论塔板为多少?
(4) 要完成本题中的分离任务,是采用普通精馏方法还是采用特殊精馏方法?试分析说明。
25℃时,在烧杯中准确加入100.0mL水样,将甘汞电极(作正极)与Ca2+选择性电极(作负极)插入溶液,测定其电动势。然后将1.00mL0.0731mol·L-1的Ca2+标准溶液加入杯中后,测得电动势降低了13.6mV。计算水样中Ca2+的浓度(mol·L-1)。
A.4:3
B.3:5
C.1:2
D.2:1
对于氧化还原反应BrO3-+5Br-+6H+====3Br2+3H2O。(1)求此反应的平衡常数;(2)计算当溶液的pH=7.0,[BrO3-]=0.10mol/L,[Br-]=0.70mol/L时,游离溴的平衡浓度。
试求将下列溶液在等温、等压下分离成纯组分所需的最小分离功:(1)含苯44%的苯-甲苯溶液;(2)含苯5%的苯一甲苯溶液;假设溶液为理想溶液,环境温度为20℃,101.3kPa条件下。
用填料塔从一混合气体中吸收所含的苯。混合气体中含苯5%(体积百分数),其余为空气,要求苯的回收率为90%(以摩尔比表示),吸收塔为常压操作,温度为25℃,入塔混合气体为每小时940(标准m3),入塔吸收剂为纯煤油,煤油的耗用量为最小耗用量的1.5倍,已知该系统的平衡关系Y=0.14X(其中Y、X为摩尔比),已知气相体积传质系数KYa=0.35kmol·m-3·s-1,纯煤油的平均相对分子质量Ms=170,塔径D=0.6m。试求:
(1) 吸收剂的耗用量为多少kg·h-1?
(2) 溶液出塔浓度X1为多少?
(3)填料层高度H为多少m?
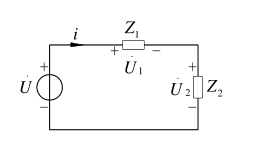
图所示电路中,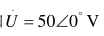 ,每一阻抗部分消耗的功率均为250W,且电压的峰值为100V。试求:(1)阻抗Z1和Z2;(2)ω=800πrad/s时电路可能含有的元件及其数值。
,每一阻抗部分消耗的功率均为250W,且电压的峰值为100V。试求:(1)阻抗Z1和Z2;(2)ω=800πrad/s时电路可能含有的元件及其数值。
一种混合液含正丁烷0.4、正戊烷0.3和正己烷0.3(均为摩尔分数),总压力为1.013×103kPa,试求:(1)混合液的泡点及平衡的汽相组成;(2)122℃下部分汽化的汽化率及汽、液相组成(压力仍为1.013×103kPa)。
A.1:1含钠溶液20ml/kg,静脉注射
B.3:2:1含钠溶液180ml/kg,静脉滴注
C.3:1含钠溶液150ml/kg,静脉滴注
D.2:1等张含钠溶液20ml/kg,静脉注射
E.4%NaHCCh溶液50ml/kg,静脎注射