 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知2,4-二甲基戊烷和苯能形成恒沸物。它们的蒸气压非常接近,例如60℃时,纯2,4-二甲基戊烷的蒸气压
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知2,4-二甲基戊烷和苯能形成恒沸物。它们的蒸气压非常接近…”相关的问题
更多“已知2,4-二甲基戊烷和苯能形成恒沸物。它们的蒸气压非常接近…”相关的问题
要求在常压下分离环己烷(1)(沸点80.8℃)和苯(2)(沸点80.2℃),它们的恒沸组成为苯0.502(摩尔分数),恒沸点77.4℃,现以丙酮为恒沸剂进行恒沸精馏,丙酮与环己烷形成恒沸物,恒沸组成为0.60(环己烷摩尔分数),若希望得到几乎纯净的苯, 试计算: (1)所需恒沸剂量; (2)塔顶、塔釜馏出物各为多少(以100kmol/h进行计算)。
已知A、B两组分在压力p=0.1MPa下所形成的均相恒沸物的组成xA=0.65(摩尔分数),在恒沸温度下纯A组分的饱和蒸气压=0.0667MPa,纯B组分的饱和蒸气压=0.018MPa。
求:
用郭氏法分析恒沸物的双塔精馏装置的设计变量数。装置的示意图如图2—17所示。
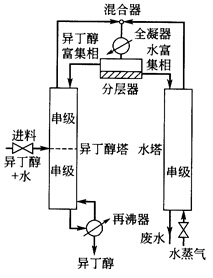 已知异丁醇塔和水塔的操作压力相同,再沸器为部分再沸器。
已知异丁醇塔和水塔的操作压力相同,再沸器为部分再沸器。
如果二元物系有最低压力恒沸物存在,则此二元物系所形成的溶液一定是( )。
a.正偏差溶液;b.理想溶液;c.负偏差溶液;d.不一定。
某二元溶液组分A、B活度系数的表达式为lnγA=0.5



A.1221
B.1227
C.1239
D.1257
用virial方程估算0.5MPa,373.15K时的等摩尔分数的甲烷(1)-乙烷(2)-戊烷(3)混合物的摩尔体积(实验值5975cm3·mol-1)。已知373.15K时的virial系数如下(单位/cm3·mol-1):B11=-20,B22=-241,B33=-621,B12=-75,B13=-122,B23=-399。
某二元系统,汽相可视为理想气体,液相为非理想溶液,溶液的超额Gibbs函数的表达式为

关于包合物的叙述错误的是()
A.包合物是一种分子被包藏在另一种分子的空穴结构内的复合物
B.包合物是一种药物被包裹在高分子材料中形成的囊状物
C.包合物能增加难溶性药物溶解度
D.包合物能使液态药物粉末化
E.包合物能促进药物稳定化