 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
将钙离子选择电极与另一参比电极浸入0.100mol·L-1Ca2+标准溶液中,参加电极为负极,于25℃测得电动势为0.250V。
将钙离子选择电极与另一参比电极浸入0.100mol·L-1Ca2+标准溶液中,参加电极为负极,于25℃测得电动势为0.250V。用未知溶液代替上述溶液时,测得电动势为0.271V,计算未知液中Ca2+的浓度。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
将钙离子选择电极与另一参比电极浸入0.100mol·L-1Ca2+标准溶液中,参加电极为负极,于25℃测得电动势为0.250V。用未知溶液代替上述溶液时,测得电动势为0.271V,计算未知液中Ca2+的浓度。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“将钙离子选择电极与另一参比电极浸入0.100mol·L-1C…”相关的问题
更多“将钙离子选择电极与另一参比电极浸入0.100mol·L-1C…”相关的问题
25℃时,用钙离子选择性电极(负极)与饱和甘汞电极(正极)组成电池,在25.0mL试液中测得电动势为0.4965V,加入2.00mL 5.45×10-2mol·L-1Ca2+标准溶液后,测得电动势为0.4117V,试求试液的p(Ca2+)。
A.10-2 :
B.10-3:
C.10-4;
D.10-5。
A.溶液中的OH-与氟化镧晶体膜中的F-进行交换;
B.溶液中的0H-破坏氟化镧晶体结构;
C.氟化镧晶体发生溶解;
D.形成氧化膜。
A.溶液中的OH-与氟化镧晶体膜中的F-进行交换;
B.溶液中的0H-破坏氟化镧晶体结构;
C.氟化镧晶体发生溶解;
D.形成氧化膜。
K(Na+,H+)=1.00×102,用该离子选择电极测定1.00×10-5mol·L-1的钠离子时,如果要控制相对误差值不大于1%,计算试液允许的pH为多大?
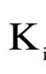 =1.8×10-6,当用该电极测浓度为1.0×10-5mol/L K+、浓度为1.0×10-2mol/L Mg2+溶液时,由Mg2+引起的K+测定误差为( )
=1.8×10-6,当用该电极测浓度为1.0×10-5mol/L K+、浓度为1.0×10-2mol/L Mg2+溶液时,由Mg2+引起的K+测定误差为( )A.0.00018%
B.134%
C.1.8%
D.3.6%