 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
从手册中查得101.33kPa、25℃时,若100g水中含氨1g,则此溶液上方的氨气平衡分压为0.987kPa。已知在此组成范围内
溶液服从亨利定律,试求溶解度系数H(kmol/(m3·kPa))及相平衡常数m。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
溶液服从亨利定律,试求溶解度系数H(kmol/(m3·kPa))及相平衡常数m。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“从手册中查得101.33kPa、25℃时,若100g水中含氨…”相关的问题
更多“从手册中查得101.33kPa、25℃时,若100g水中含氨…”相关的问题
某混合气体中含有2%(体积)CO2,其余为空气。混合气体的温度为30℃,总压强为506.6kPa。从手册中查得30℃时CO2在水中的亨利系数E=1.88×105kPa,试求溶解度系数H(kmol/(m3·kPa))及相平衡常数m,并计算每100克与该气体相平衡的水中溶有多少克CO2。
一低频功率晶体管LM3886,由手册查得R(th)jc=1℃/W,R(th)ca=36℃/W,TjM=165℃,装置散热片后,若R(th)cs=0.5℃/W,R(th)sa=1.5℃/W,试求Ta0=25℃及Ta=60℃时采用散热片前后的最大允许管耗PCM,并进行分析。
将2500kg·h-1NaOH水溶液在一单效蒸发器内从10%(质量分数,下同)蒸发浓缩到25%。已知加热蒸汽的绝对压力为450kPa,蒸发室内的压力为101.33kPa,溶液的沸点为115℃,比定压热容为3.9kJ·kg-1·℃-1,热损失为20kW。试计算:
(1) 进料温度为20℃时,所需加热蒸汽消耗量和单位蒸汽消耗量;
(2) 沸点进料时,所需加热蒸汽消耗量和单位蒸汽消耗量。
在单效蒸发器中,每小时将10000kg的NaNO3水溶液从5%浓缩到25%。原料液温度为40℃。分离室的真空度为60kPa,加热蒸汽表压为30kPa。蒸发器的总传热系数为2000W/(m2·℃),热损失很小可以略去不计。试求蒸发器的传热面积及加热蒸汽消耗量。设液柱静压强引起的温度差损失可以忽略。当地大气压强为101.33kPa。
在逆流操作的吸收塔中,于101.33kPa、25℃下用清水吸收混合气中的H2S,将其组成由2%降至0.1%(体积)。该系统符合亨利定律。亨利系数E=5.52×104kPa。若取吸收剂用量为理论最小用量的1.2倍,试计算操作液气比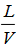 及出口液相组成X1。若压强改为1013kPa,其他条件不变,再求
及出口液相组成X1。若压强改为1013kPa,其他条件不变,再求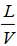 及X1。
及X1。
温度为25℃、总压为101.3kPa时,查得CO2的亨利系数E=14.39×104kPa。试计算:
(1) 溶解度系数H及相平衡常数m的值(对稀水溶液ρ=998kg·m-3);
(2) 若CO2在空气中的分压为10.13kPa,求与其成平衡的水溶液浓度,分别以摩尔分数和kmol·m-3表示。
在总压101.33kPa下,已知湿空气的某些参数,利用湿空气的H-I图查出本题表10-2中空格内的数值,并给出序号4中各数值的求解过程示意图。
表10-2 | |||||||
序号 | 干球温度 | 湿球温度 | 湿度kg/kg绝干气 | 相对湿度% | 焓kJ/kg绝干气 | 水汽分压kPa | 露点℃ |
1 | (60) | (35) | |||||
2 | (40) | (25) | |||||
(20) | (75) | ||||||
4 | (30) | (4) |
查得总压为101.3kPa,温度为25℃时,在100g水中含氨1g,该溶液上方蒸汽的平衡分压p*为0.986kPa。已知在此浓度范围内,该溶液服从亨利定律,稀氨水溶液的密度可按纯水计算。试求溶解度系数H[以kmol/(m3·kPa)为单位]和相平衡系数m。
(2008年)水蒸气的干度为x:从水蒸气表中查得饱和水的焓为h,湿饱和蒸汽的焓为h",计算湿蒸汽焓的表达式是()。
A.hx=h"+x(h"-h")
B.hx=x(h"-h")
C.hxh"-x(h"-h")
D.hx=h"+x(h"-h")