 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在1 mol·L-1 H2SO4溶液中,Ce4+/Ce3+的条件电位为1.44 V;Fe3+/Fe2+的条件电位为0.68V;以Ce4+滴定F
A.二苯胺磺酸钠(条件电位0.84 V)
B.邻苯氨基苯甲酸(条件电位0.89 V)
C.邻二氮菲-亚铁(条件电位1.06 V)
D.硝基邻二氮菲-亚铁(条件电位1.25 V)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.二苯胺磺酸钠(条件电位0.84 V)
B.邻苯氨基苯甲酸(条件电位0.89 V)
C.邻二氮菲-亚铁(条件电位1.06 V)
D.硝基邻二氮菲-亚铁(条件电位1.25 V)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在1 mol·L-1 H2SO4溶液中,Ce4+/Ce3+的…”相关的问题
更多“在1 mol·L-1 H2SO4溶液中,Ce4+/Ce3+的…”相关的问题
1.000LK2Cr2O7溶液中含24.52gK2Cr2O7,则c(1/6K2Cr2O7)______mol·L-1。已知M(K2Cr2O7)=294.18g·mol-1。
PbSO4和为1.8×10-8,在纯水中其溶解度为______mol·L-1;在浓度为1.0×10-2mol·L-1的Na2SO4溶液中达到饱和时其溶解度为______mol·L-1。
今欲配制pZn为11.0的溶液,若控制pH=5.5,在20mL 0.020mol·L-1Zn2+溶液中应加入同体积浓度为______mol·L-1的EDTA溶液。(lgKZnY=16.5;pH=5.5时,lgαY(H)=5.5。)
现有100mL浓度为3mol·L-1的H2SO4(相对分子质量为98)溶液,密度ρ=1.18g·mL-1,取出10mL放在干燥烧杯中。烧杯中溶液的浓度c(H2SO4)=______,H2SO4的质量分数为______,烧杯中溶液含溶质的物质的量n(H2SO4)=______。
,然后用 0.03000 mol·L-1 K2Cr2O7溶液滴定,用去25.00 mL。计算试样中FeO和Al2O3的质量分数
含有0.010mol·L-1Mg-EDTA配合物的pH=10的氨性溶液中,[Mg2+]=______mol·L-1,[Y4-]=______mol·L-1。(lgKMgY=8.7;pH=10时,lgαY(H)=0.45)
含有0.01mol·L-1Mg-EDTA配合物的pH=10的氨性溶液中,ce(Mg2+)=______mol·L-1,ce(Y4-)=______mol·L-1。[lg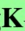 (MgY)=8.7,pH=10时,lgαY(H)=0.45]
(MgY)=8.7,pH=10时,lgαY(H)=0.45]
在pH值为10.0的氨性溶液中,含Zn2+和Mg2+各0.020mol·L-1,用0.020mol·L-1EDTA溶液滴定Zn2+时,Mg2+是否干扰测定:______(填是与否)。若有干扰,应如何改变滴定条件:______。(设△pZn'=0.2,并要求滴定误差|Et|≤0.3%;已知化学计量点时[NH3]=0.20 mol·L-1,lgKZnY=16.5,lgKMgY=8.7。)
25℃时,在烧杯中准确加入100.0mL水样,将甘汞电极(作正极)与Ca2+选择性电极(作负极)插入溶液,测定其电动势。然后将1.00mL0.0731mol·L-1的Ca2+标准溶液加入杯中后,测得电动势降低了13.6mV。计算水样中Ca2+的浓度(mol·L-1)。
用Cl-选择性电极作负极,SCE作正极组成电池,测定某溶液中氯化物的含量。取100mL此溶液在25℃时测得电池电动势为28.8mV,加入1.00mL浓度为0.475mol·L-1的经酸化的NaCl标准溶液后,测得电池电动势为53.5mV。求该溶液中氯化物的浓度(mol·L-1)。
下表所列为某酶在一组底物浓度不同的,反应中测得的反应速度:
| [S] (mmol·L-1) | v (μmol·L-1·分-1) | [S] (mmol·L-1) | v (μmol·L-1·分-1) |
| 1.3×10-5 1.5×10-4 2.0×10-4 | 12 45 48 | 2.0×10-3 2.0×10-2 2.0×10-1 | 60 60 60 |
求: