 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知水的表面张力与温度的关系式为 γ=(75.64-0.00495T/K)×10-3N·m-1 在283K时,可逆地使一定量纯水的表面
已知水的表面张力与温度的关系式为
γ=(75.64-0.00495T/K)×10-3N·m-1
在283K时,可逆地使一定量纯水的表面积增加0.01m2(设体积不变),求系统的如下各量:ΔU、△H、△S、△A、AG、Q和W。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知水的表面张力与温度的关系式为
γ=(75.64-0.00495T/K)×10-3N·m-1
在283K时,可逆地使一定量纯水的表面积增加0.01m2(设体积不变),求系统的如下各量:ΔU、△H、△S、△A、AG、Q和W。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知水的表面张力与温度的关系式为 γ=(75.64-0.00…”相关的问题
更多“已知水的表面张力与温度的关系式为 γ=(75.64-0.00…”相关的问题
在101.325kPa压力下,若水中只含有直径为10-6m的空气泡,那么这样的水在什么温度下才能沸腾?已知水在373K的表面张力σ=58.9×10-3N/m,摩尔气化热△vapHm=40.656kJ/mol。设水面至空气泡之间液柱的静压力及气泡内蒸汽压下降等因素均可忽略不计。
雾的粒子质量约为1×10-12g,试求20℃时其饱和蒸气压与平面水的饱和蒸气压之比。已知20℃时水的表面张力为72.75×10-3N·m-1,体积质量(密度)为0.9982g·cm-3,H2O的摩尔质量为18.02g·mol-1。
从饱和Weston电池的电动势与温度的关系式,试求298.15K,当电池产生2mol电子的电荷量时,电池反应的△rGm、△rHm和△rSm。已知该关系式为
E/V=1.01845-4.05×10-5(T/K-293.15)-9.5×10-7(T/K-293.15)2
常用的铅蓄电池可表示为Pb(s)|PbSO4(s)|H2SO4(m=1mol·kg-1)|PbSO4(s)|PbO2(s)|Pb(s)。已知在0~60℃的温度区内,电动势与温度的关系式为
E/V=1.91737+56.1×10-6(t/℃)+1.08×10-8(t/℃)2
在25℃时,电池的摩尔电压=2.041V,试计算这时电解质溶液H2SO4(m=1mol·kg-1)的平均活度因子γ±。
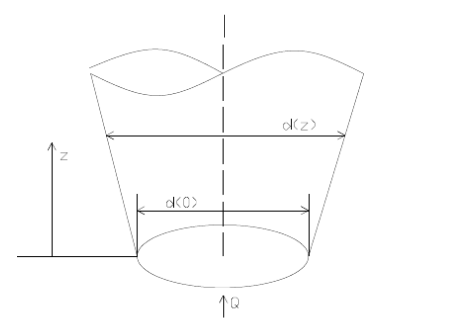
如图所示,水在变径竖管中从下往上流动,已知z=0处的直径d(0)=0.5m,通过的流量Q=0.9m3/s,不计粘性作用,为使管中各断面的压力相同,即p(z)=p(0),试求竖管的直径d(z)与z的关系式。
已知293K时水的表面张力为0.07275N·m-1,汞的表面张力为0.470N·m-1,汞-水间的界面张力为0.375N·m-1,试判断水能否在汞的表面铺展?
水蒸气迅速冷却至298K会发生过饱和现象。已知298K时水的表面张力为72.1×10-3N/m,密度为997kg/m3。当过饱和水蒸气压为水的平衡蒸汽压的4倍时,试求算最初形成的水滴半径为多少?此种水滴中含有多少个水分子?
 .
.
已知水在77℃时的饱和蒸气压为41.891kPa,水在101.325kPa下的正常沸点为100℃,求:
(1)下面表示水的蒸气压与温度关系的方程式中的A和B值:
lgp=-A/T+B
(2)在此温度范围内水的摩尔蒸发焓;
(3)在多大压力下水的沸点为105℃。
由组分A与B组成的溶液,液相活度系数与组成的关联式为: ,已知90℃时,纯物质的饱和蒸气压分别为
,已知90℃时,纯物质的饱和蒸气压分别为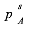 =133.289kPa,
=133.289kPa,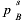 =93.303kPa,系统符合低压气液平衡的关系式,试求:
=93.303kPa,系统符合低压气液平衡的关系式,试求:
雾是由许多微小球形水滴组成的,其直径约为10-6m。由于表面张力的作用,在水滴内的压力比其外压要大,其19的压差可用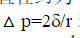 表示,式中,δ代表水的表面张力,7为液滴的半径。25℃时水的表面张力为0.0694N·m-1。由于水滴内的压力大,会使雾滴不稳定而消失。问:(1)要使雾滴稳定,滴内的温度应比表面水低多少?(2)雾滴在大气中形成,水的逸度也会因含有杂质而降低,至少溶解多少杂质才能使雾滴在25℃时不再消失?(设其服从Lewis-Randall规则。)
表示,式中,δ代表水的表面张力,7为液滴的半径。25℃时水的表面张力为0.0694N·m-1。由于水滴内的压力大,会使雾滴不稳定而消失。问:(1)要使雾滴稳定,滴内的温度应比表面水低多少?(2)雾滴在大气中形成,水的逸度也会因含有杂质而降低,至少溶解多少杂质才能使雾滴在25℃时不再消失?(设其服从Lewis-Randall规则。)