 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
等温下进行1.5级液相不可逆反应A→B+C,反应速率常数为5m1.5/(kmol1.5·h),A的浓度为2kmol/m3,进入反应装置的
等温下进行1.5级液相不可逆反应A→B+C,反应速率常数为5m1.5/(kmol1.5·h),A的浓度为2kmol/m3,进入反应装置的流量为1.5m3/h。试分别计算下列情况下A的转化率达95%时所需的反应体积。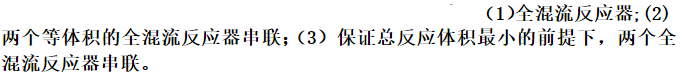
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
等温下进行1.5级液相不可逆反应A→B+C,反应速率常数为5m1.5/(kmol1.5·h),A的浓度为2kmol/m3,进入反应装置的流量为1.5m3/h。试分别计算下列情况下A的转化率达95%时所需的反应体积。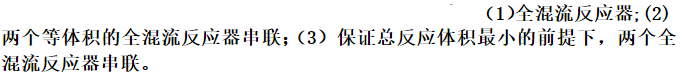
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“等温下进行1.5级液相不可逆反应A→B+C,反应速率常数为5…”相关的问题
更多“等温下进行1.5级液相不可逆反应A→B+C,反应速率常数为5…”相关的问题
在间歇反应器中等温进行下列液相反应
A+B→R rR=1.6cA[kmol/(m3·h)]
2A→D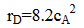 [kmol/(m3·h)]
[kmol/(m3·h)]
式中,rR,rD分别为产物R和D的生成速率。反应用的原料为A与B的混合液,其中A的浓度为2kmol/m3。

反应器体积的计算
例: PFR与间歇反应器的比较
在容积为2.5m3的理想间歇反应器中进行液相反应
A+B→P
反应维持在75℃等温操作,实验测得反应速率方程式为
(-rA)=kcAcBkmol/(L·s)
k=2.78×10-3L/(mol·s),当反应物A和B的初始浓度cA0=cB0=4mol/L,而A的转化率xA=0.8时,该间歇反应器平均每分钟可处理0.684kmol的反应物A。今若将反应移到一个管径为125mm的理想管式反应器中进行,仍维持75℃等温操作,且处理量和所要求转化率相同,求所需反应器的管长。
设在给定的T、p下,某特定二元系的液相摩尔体积符合下列关系式:
V=100x1+80x2+2.5x1·x2(cm3·mol-1)
(1)导出偏摩尔体积
要在一个板式塔中用清水吸收混于空气中的丙酮蒸气。混合气体流量为30kmol/h,其中含丙酮1%(体积)。要求吸收率达到90%,用水量为90kmol/h。该塔在101.33kPa、27℃下等温操作,丙酮在气、液两相中的平衡关系为Y*=2.53X,求所需理论板数。
水-异丁醇系统液相部分互溶。在101.325kPa下,系统的共沸点为89.7℃。气(G)、液(L1)、液(L2)三相平衡时的组成ω(异丁醇)依次为:70.0%,8.7%,85.0%。今由350g水和150g异丁醇形成的系统在101.325kPa压力下由室温加热,问:(1)温度刚要达到共沸点时,系统处于相平衡时存在哪些相?其质量各为多少?(2)当温度由共沸点刚有上升趋势时,系统处于相平衡时存在哪些相?其质量各为多少?
某二元系统,汽相可视为理想气体,液相为非理想溶液,溶液的超额Gibbs函数的表达式为

某一气相反应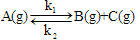 ,已知在298 K时,k1=0.21s-1,k-2=5×10-9Pa-1·s-1,当温度由298K升到310K时,k1和k-2的值均增加1倍,试求:
,已知在298 K时,k1=0.21s-1,k-2=5×10-9Pa-1·s-1,当温度由298K升到310K时,k1和k-2的值均增加1倍,试求:
(1)298K时的反应平衡常数Kp
(2)正,逆反应的实验活化能Ea
和200.0g苯置于带活塞的导热容器中,始态为一定压力下90℃的液态混合物。在恒温90℃下逐渐降低压力,问:(1)压力降到多少时,开始产生气相,此气相的组成如何?(2)压力降到多少时,液相开始消失,最后一滴液相的组成如何?(3)压力为92.00kPa时,系统内气一液两相平衡,两相的组成如何?两相的物质的量各为多少?
在总压101.33kPa、温度350.8K下,苯(1)-正已烷(2)形成x1=0.525的恒沸混合物。此温度下两组分的蒸气压分别是99.4kPa和97.27kkPa,液相活度系数模型选用Margules方程,气相服从理想气体,求:350.8K下的气液平衡关系p-x1和y1-x1的函数式。