 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知反应2SO2+O2====2SO3在1062K时的,如果在该温度下,于某一容器中含有SO2,O2,SO3三种气体,其分压力分别为:
已知反应2SO2+O2====2SO3在1062K时的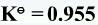 ,如果在该温度下,于某一容器中含有SO2,O2,SO3三种气体,其分压力分别为:p(SO2)=30.4kPa,P(O2)=60.1kPa,P(SO3)=25.3kPa。试判断反应进行的方向。
,如果在该温度下,于某一容器中含有SO2,O2,SO3三种气体,其分压力分别为:p(SO2)=30.4kPa,P(O2)=60.1kPa,P(SO3)=25.3kPa。试判断反应进行的方向。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知反应2SO2+O2====2SO3在1062K时的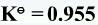 ,如果在该温度下,于某一容器中含有SO2,O2,SO3三种气体,其分压力分别为:p(SO2)=30.4kPa,P(O2)=60.1kPa,P(SO3)=25.3kPa。试判断反应进行的方向。
,如果在该温度下,于某一容器中含有SO2,O2,SO3三种气体,其分压力分别为:p(SO2)=30.4kPa,P(O2)=60.1kPa,P(SO3)=25.3kPa。试判断反应进行的方向。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知反应2SO2+O2====2SO3在1062K时的,如果…”相关的问题
更多“已知反应2SO2+O2====2SO3在1062K时的,如果…”相关的问题
的反应速率之间的关系。
(1)N2+3H2→2NH3
(2)2SO2+O2→2SO3
(3)aA+bB→gG+hH
下列反应中,
(A) C(s)+O2(g)→CO2(g);
(B) 2SO2(g)+O2(g)→2SO3(g);
(C) 3H2(g)+N2(g)→2NH3(g);
(D) CuSO4(s)+5H2O(l)→CuSO4·5H2O(s)。
 值最大的是( )
值最大的是( )A.C(s)+O2(g)→CO2(g)
B.2SO2(g)+O2(g)→2SO3(g)
C.CaSO4(s)+2H2O(l)→CaSO4·2H2O(s)
D.3H2(g)+N2(g)→2NH3(g)
N2O5分解反应N2O5→2NO2+1/2O2是一级反应,已知其在某温度下的速率常数为4.8×10-4s-1。

在间歇反应器中等温下进行下列反应:
两个反应对各反应物均为一级反应,已知在反应温度下,
试计算CH3NH2的最大收率及相应的NH3的转化率。
已知ΔfGm(NH3,g)=-16.45kJ·mol-1,计算合成氨反应
N2(g)+3H2(g)→2NH3(g)
在298.15K、标准状态时反应的标准平衡常数KΘ。
已知反应2NO+O2====2NO2为三级反应。下列操作会使反应速率常数改变的是
(A) 减小体系的压力; (B) 在反应体系中加入大量的NO;
(C) 降低反应温度; (D) 在反应体系中加入NO2。
已知在1000K,理想气体反应A(s)+B2C(g)====AC(s)+B2(g)的
已知某药物按一级反应分解,在体温37℃时,反应速率常数为0.36h-1。若服用该药物0.20g,问该药物在胃中停留多长时间方可分解80%?