 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
容器中放有100g N2,温度与压力分别为25℃和3039.75kPa,若该气体反抗1013.25kPa压力等外压绝热膨胀,试计算系
容器中放有100g N2,温度与压力分别为25℃和3039.75kPa,若该气体反抗1013.25kPa压力等外压绝热膨胀,试计算系统的最终温度T和过程的△U、△H。假定N2是理想气体,且CV,m=20.71J·mol-1·K-1。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
容器中放有100g N2,温度与压力分别为25℃和3039.75kPa,若该气体反抗1013.25kPa压力等外压绝热膨胀,试计算系统的最终温度T和过程的△U、△H。假定N2是理想气体,且CV,m=20.71J·mol-1·K-1。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“容器中放有100g N2,温度与压力分别为25℃和3039.…”相关的问题
更多“容器中放有100g N2,温度与压力分别为25℃和3039.…”相关的问题
统所能达到的最高温度和最大压力。空气组成按y(O2,g)=0.21,y(N2,g)=0.79计算。水蒸气的标准摩尔生成焓见附录(在教材中)。各气体的平均摩尔定容热容分别为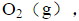
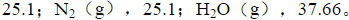 假设气体适用于理想气体状态方程。
假设气体适用于理想气体状态方程。
1molH2与过量50%空气混合物的始态为25℃、101.325kPa。若该混合气体于容器中发生爆炸,试求所能达到的最高爆炸温度与压力。设所有气体均可按理想气体处理。H2O(g)、O2及N2的平均定容摩尔热容分别为37.66J·mol-1·K-1、25.1J·mol-1·K-1及25.1J·mol-1·K-1。
A(g)按下式分解:A(g) 2B(g)。
2B(g)。
(1)在298K时,0.5dm3容器中装有1.588×10-3kg的A(g),平衡时总压力为100kPa。试判断298K,A(g)和B(g)的分压各为150kPa时,上述反应能否自发进行?
(2)若在318K、0.5dm3容器中放入1.35×10-3kg的A(g)时,平衡总压力为105kPa。已知该反应的反应焓与温度的关系为
已知:MA=92.02×10-3kg·mol-1,

1mol N2(g)可看做理想气体,从始态298K、100kPa,经如下两个等温过程,分别到达终态压力为600kPa,分别求过程的Q、W、△U、△H、△A、△G、△S和△Siso。
(1)等温可逆压缩;
(2)等外压为600kPa时压缩。
把压力为700kPa,温度为5℃的空气装于0.5m3的容器中,加热使容器中的空气温度升至115℃。在这个过程中,空气由一小洞漏出,使压力保持在700kPa,试求热传递量。
把压力为700kPa,温度为5℃的空气装于0.5m3的容器中,加热使容器中的空气温度升至115℃。在这个过程中,空气由一小洞漏出,使压力保持在700kPa,试求热传递量。
在容积为2m3的容器中水占1/10,其余为蒸汽,温度为150℃,试确定容器中工质的质量及压力。
合成氨反应为3H2(g)+N2(g)∩2NH3(g),所用反应物氢气和氮气的摩尔比为3:1,在673K、1000kPa压力下达成平衡,平衡产物中氨的摩尔分数为0.0385。试求:(1)该反应在该条件下的标准平衡常数;(2)在该温度下,若要使氨的摩尔分数为0.05,应控制总压为多少。
压力P1=2MPa,温度t1=400℃的蒸汽,经节流阀后,压力降为P1'=1.6MPa,再经喷管射入压力为Pb=1.2MPa的大容器中,若喷管出口截面积A2=200mm2。

输气管内的参数维持常数,压力为p、温度为t、焓为h。储气罐中原有的空气质量m1,热力学能u1,压力p1,温度T1(如图所示)。充气后,储气罐内空气质量为m2,热力学能u2,忽略动能差与位能差,且容器为刚性绝热。导出u2与h的关系式。
