 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应①H2O(g), ②CO(g), (1)在标准状态下,用C(石墨)还原水制H2(g)和CO(g)的最低温度; (2)在1073K、100kPa条
反应① H2O(g),
H2O(g),
② CO(g),
CO(g),
(1)在标准状态下,用C(石墨)还原水制H2(g)和CO(g)的最低温度;
(2)在1073K、100kPa条件下用C(石墨)还原水制H2(g)和CO(g)系统的平衡气相组成为多少?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应① H2O(g),
H2O(g),
② CO(g),
CO(g),
(1)在标准状态下,用C(石墨)还原水制H2(g)和CO(g)的最低温度;
(2)在1073K、100kPa条件下用C(石墨)还原水制H2(g)和CO(g)系统的平衡气相组成为多少?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“反应①H2O(g), ②CO(g), (1)在标准状态下,用…”相关的问题
更多“反应①H2O(g), ②CO(g), (1)在标准状态下,用…”相关的问题
反应CO(g)+H2O(g)==H2(g)+CO2(g)的标准平衡常数与温度的关系为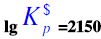 K/T-2.216,当CO、H2O、H2、CO2的起初组成的质量分数分别为0.30、0.30、0.20和0.20,总压为101.3kPa时,在什么温度以下(或以上)反应向生成产物的方向进行?
K/T-2.216,当CO、H2O、H2、CO2的起初组成的质量分数分别为0.30、0.30、0.20和0.20,总压为101.3kPa时,在什么温度以下(或以上)反应向生成产物的方向进行?
已知同一温度,两反应方程及标准平衡常数如下:
(1) C(石墨)+H2O(g)===CO(g)+H2(g)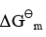
(2) C(石墨)+2H2O(g)===CO2(g)+2H2(g)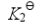
求反应CO(g)+H2O(g)===CO2(g)+H2(g)的KΘ。
已知在温度为298.15K的标准条件下,CO(g)和H2O(g)的标准摩尔生成焓分别为-110.53kJ/mol和-241.83kJ/mol。计算反应H2O(g)+C(石墨)====CO(g)+H2(g)的标准摩尔焓变。
1mol液态苯完全燃烧生成CO2(g)和H2O(l),则该反应的Qp与QV的差值为______kJ·mol-1(25℃)。
 N2(g)+CO2(g)
N2(g)+CO2(g) <0。欲使有害气体NO、CO尽可能转化为N2和CO2,应采取的条件为:
<0。欲使有害气体NO、CO尽可能转化为N2和CO2,应采取的条件为:A.低温高压;
B.高温高压;
C.低温低压;
D.高温低压。
反应2NaHCO3(s)===Na2CO3(s)+H2O(g)+CO2(g)在不同温度时的平衡总压如表5-3所示。
表5-3 | ||||||
t/℃ | 30 | 50 | 70 | 90 | 100 | 110 |
p/kPa | 0.827 | 3.999 | 15.90 | 55.23 | 97.47 | 167.0 |
设反应的Δr Hm与温度无关。
求:(1)上述反应的ΔrHm;
(2)lg(p/kPa)与T的函数关系;
(3)NaHCO3(s)的分解温度。
在100℃下,反应COCl2(g)===CO(g)+Cl2(g)的KΘ=8.1×10-9,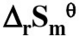 =125.6J·mol-1·K-1。计算:(1)100℃,总压力为200kPa时COCl2的离解度;(2)100℃下上述反应的
=125.6J·mol-1·K-1。计算:(1)100℃,总压力为200kPa时COCl2的离解度;(2)100℃下上述反应的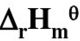 ;(3)总压力为200kPa,COCl2的解离度为0.1%时的温度。设△rCp,m=0。
;(3)总压力为200kPa,COCl2的解离度为0.1%时的温度。设△rCp,m=0。
随温度升高,反应(1):2M(s)+O2(g)=2MO(s)和反应(2):2C(s)+O2(g)=2CO(g)的摩尔吉布斯自由能升高的为______,降低的为______,因此,金属氧化物MO被碳还原反应MO(s)+C(s)=M(s)+CO(g)在高温条件下______向自发。
已知化学反应式CH4(g)+CO2(g)===2CO(g)+2H2(g):

(3)25℃时,若始态CH4(g)和CO2(g)的分压均为150kPa,末态CO(g)和H2(g)的分压均为50kPa,求反应的△rSm和△rGm。
已知化学反应式CH4(g)+CO2(g)===2CO(g)+2H2(g):
(1)利用附录(在教材中)中各物质的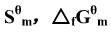 ,数据,求上述反应在25℃时的
,数据,求上述反应在25℃时的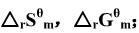
;(2)利用附录(在教材中)中各物质的△rGm数据,求上述反应在25℃时的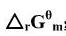 ;
;
(3)25℃时,若始态CH4(g)和CO2(g)的分压均为150kPa,末态CO(g)和H2(g)的分压均为50kPa,求反应的△rSm和△rGm。