 更多“在用pH玻璃电极测定溶液pH时,为什么要选用与待测试液pH相…”相关的问题
更多“在用pH玻璃电极测定溶液pH时,为什么要选用与待测试液pH相…”相关的问题
第1题
pH玻璃电极与饱和甘汞电极组成如下电池:玻璃电极|H+(x)‖饱和甘汞电极。测定pH为4.01的邻苯二甲酸氢钾缓冲溶
pH玻璃电极与饱和甘汞电极组成如下电池:玻璃电极|H+(x)‖饱和甘汞电极。测定pH为4.01的邻苯二甲酸氢钾缓冲溶液时,其电池电动势为0.211V。而测定两个未知溶液时,其电池电动势分别为0.435V和0.0186V,试计算两种未知溶液的pH(25℃)。
第4题
用玻璃电极作指示电极,以0.200mol·L-1苯甲酸溶液,从滴定曲线上求得终点时溶液的pH为8.22,二分之一终点时溶
用玻璃电极作指示电极,以0.200mol·L-1苯甲酸溶液,从滴定曲线上求得终点时溶液的pH为8.22,二分之一终点时溶液pH为4.18,试计算苯甲酸的解离常数。
第5题
用pH玻璃电极为指示电极,以0.2000mol·L-1NaOH溶液滴定0.02000mol·L-1苯甲酸溶液。从滴定曲线上求得终点时pH=8.22,二分之一终点时溶液的pH=4.18,则苯甲酸的Ka为______。
A.6.0×10-9;
B.6.6×10-5;
C.6.6×10-9;
D.数据少无法确定。
第6题
25℃时,用pH=4.00的标准缓冲溶液,测得电池:“玻璃电极|H+(a=Xmol·L-1)‖饱和甘汞电极”的电动势为0.814V,那么在
25℃时,用pH=4.00的标准缓冲溶液,测得电池:“玻璃电极|H+(a=Xmol·L-1)‖饱和甘汞电极”的电动势为0.814V,那么在c(HAc)=1.00×10-3mol·L-1的醋酸溶液中,此电池的电动势为多少?(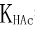 =1.8×10-5,设a(H+)=[H+])
=1.8×10-5,设a(H+)=[H+])
第10题
K(Na+,H+)=1.00×102,用该离子选择电极测定1.00×10-5mol·L-1的钠离子时,如果要控制相对误差值不大于1%,计算
K(Na+,H+)=1.00×102,用该离子选择电极测定1.00×10-5mol·L-1的钠离子时,如果要控制相对误差值不大于1%,计算试液允许的pH为多大?
第11题
玻璃电极的膜电位______。
A.随溶液中氢离子活度的增高向负方向移动;
B.随溶液中氢离子活度的增高向正方向移动;
C.随溶液中氢氧根离子活度的增高向正方向移动;
D.随溶液pH的增高向正方向移动。


 如果结果不匹配,请
如果结果不匹配,请 

















