 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列化合物BF3、CCl4、H2O、CO2的键角由小到大的顺序是______。
下列化合物BF3、CCl4、H2O、CO2的键角由小到大的顺序是______。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列化合物BF3、CCl4、H2O、CO2的键角由小到大的顺序是______。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列化合物BF3、CCl4、H2O、CO2的键角由小到大的顺…”相关的问题
更多“下列化合物BF3、CCl4、H2O、CO2的键角由小到大的顺…”相关的问题
下列化合物中中心原子采用sp3杂化方式的是( )。
(A) H2O (B) CCl4(C) NH3(D) 以上都是
根据分子几何构型和成键原子的电负性说明下列各对分子的偶极矩大小:
(1)HCl,HBr;
(2)CO2,SO2;
(3)CCl4,CH4;
(4)NH3,PH3;
(5)BF3,NF3;
下列关于BF3的叙述中,正确的是
(A) BF3易形成二聚体; (B) BF3为离子化合物;
(C) BF3为路易斯酸; (D) BF3常温下为液体。
将下列两组物质按沸点由低到高的顺序排列,并说明理由。
(1) H2CO Ne HF (2) CI4CF4CBr4CCl4
判断下列分子之间存在什么形式的分子间作用力:
H2S气体;CH4气体;He气体;NH3气体;H2与H2O;CH3Cl液体;NH3液体;C6H6与CCl4;C2H5OH和H2O;C2H5OH和C2H5OC2H5;HBr气体;CO2气体。
根据配合物的价键理论,指出下列配离子其中心离子的电子排布、杂化轨道的类型和配离子的空间构型。
[Mn(H2O)6]2+[Ag(CN)2] [Cd(NH3)4]2+[Ni(CN)4]2-[Co(NH3)6]3+
通过计算判断下列化合物是否符合EAN规则。 (1)K[Pt(C2H4)Cl3]; (2)Ru(C5H5)2; (3)Mo(CO)6; (4)K4[Fe(CN)6]; (5)V(CO)6; (6)Mn2(CO)10。
已知同一温度,两反应方程及标准平衡常数如下:
(1) C(石墨)+H2O(g)===CO(g)+H2(g)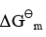
(2) C(石墨)+2H2O(g)===CO2(g)+2H2(g)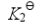
求反应CO(g)+H2O(g)===CO2(g)+H2(g)的KΘ。
反应CO(g)+H2O(g)==H2(g)+CO2(g)的标准平衡常数与温度的关系为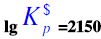 K/T-2.216,当CO、H2O、H2、CO2的起初组成的质量分数分别为0.30、0.30、0.20和0.20,总压为101.3kPa时,在什么温度以下(或以上)反应向生成产物的方向进行?
K/T-2.216,当CO、H2O、H2、CO2的起初组成的质量分数分别为0.30、0.30、0.20和0.20,总压为101.3kPa时,在什么温度以下(或以上)反应向生成产物的方向进行?
已知在温度为298.15K的标准条件下,CO(g)和H2O(g)的标准摩尔生成焓分别为-110.53kJ/mol和-241.83kJ/mol。计算反应H2O(g)+C(石墨)====CO(g)+H2(g)的标准摩尔焓变。
反应① H2O(g),
H2O(g),
② CO(g),
CO(g),
(1)在标准状态下,用C(石墨)还原水制H2(g)和CO(g)的最低温度;
(2)在1073K、100kPa条件下用C(石墨)还原水制H2(g)和CO(g)系统的平衡气相组成为多少?