题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对于有过量KI存在的AgI溶胶,哪一种电解质的聚沉能力最强( )。
A.K3[Fe(CN)6]
B.MgSO4
C.FeCl3
D.MgCl2
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.K3[Fe(CN)6]
B.MgSO4
C.FeCl3
D.MgCl2
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“对于有过量KI存在的AgI溶胶,哪一种电解质的聚沉能力最强(…”相关的问题
更多“对于有过量KI存在的AgI溶胶,哪一种电解质的聚沉能力最强(…”相关的问题
以KI和AgNO3为原料制备AgI溶胶时,如果KI过量,则制得的AgI胶团结构式为:______;若AgNO3过量,则制得的AgI胶团结构式为______。
试通过计算说明,向含有Ag2CrO4固体的溶液中加入KI溶液有何现象产生?
已知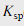 Ag2CrO41.1×10-12,AgI 8.5×10-17。
Ag2CrO41.1×10-12,AgI 8.5×10-17。
如将50mgAgCl溶解在10mL3mol·L-1的NH3·H2O中,再加入10mL0.05mol·L-1的KI溶液,有无AgI沉淀产生?(已知Ksp(AgI)=8.3×10-17,
将0.1963g分析纯K2Cr2O7试剂溶于水,酸化后加入过量KI,析出的I2需用33.61mLNa2S2O3溶液滴定。计算Na2S2O3溶液的浓度。
无色晶体A溶于NaOH溶液后加热有无色气体B放出。将B通入AgNO3溶液先有棕黑色沉淀析出,过量后黑色沉淀溶解得无色溶液C。向C中加入盐酸有白色沉淀D生成。向A的水溶液中加入KI溶液则溶液变黄,再加入BaCl2溶液则有不溶于酸的白色沉淀E生成。试确定A,B,C,D,E各为何物质?
用间接碘量法测定BaCl2的纯度时,先将Ba2+沉淀为Ba(IO3)2,洗涤后溶解并酸化,加入过量的KI,然后用Na2S2O3标准溶液滴定,此处BaC12与Na2S2O3的计量关系[n(BaC12):n(Na2S2O3)]为()。
A.1:2
B.1:3
C.1:6
D.1:12
浓度均为0.0100mol·L-1的Zn2+、Cd2+混合溶液,加入过量KI,使终点时游离I-浓度为1mol·L-1,在pH=5.0时,以二甲酚
浓度均为0.0100mol·L-1的Zn2+、Cd2+混合溶液,加入过量KI,使终点时游离I-浓度为1mol·L-1,在pH=5.0时,以二甲酚橙(XO)为指示剂,用等浓度的EDTA滴定其中的Zn2+,计算终点误差。(lgKZnY=16.50,lgKCdY=16.46;pH=5.0时,lgαY(H)=6.45、lgK'Zn-XO=4.8;Cd2+-I-络合物的Igβ1~lgβ4分别为2.10、3.43、4.49、5.41)
称取含BaCl2试样0.5000g,溶于水后加25.00mL 0.05000mol/L KIO3将Ba2+沉淀为Ba(IO3)2,滤去沉淀,洗涤,加入过量KI于滤液中并酸化,滴定析出的I2,消耗0.1000mol/L的Na2S2O3标准溶液21.18mL。写出有关反应方程式,计算BaCl2的百分含量?(MBaCl2=208.27)
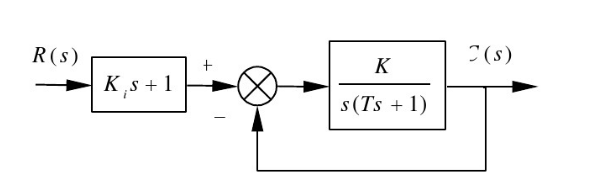
随动控制系统的方框图如图所示。若输入信号为r(t)=at(a为任意常数)。试证明通过适当地调节Ki的值,该系统对于斜坡输入的响应的稳态误差能达到零。