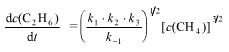题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
双环戊烯单分子气相热分解反应,在483K时的速率常数k(483K)=2.05×10-4s-1,在545K时的速率常数k(545K)=1.86×1
双环戊烯单分子气相热分解反应,在483K时的速率常数k(483K)=2.05×10-4s-1,在545K时的速率常数k(545K)=1.86×10-2s-1。已知kB=1.38×10-23J·K-1,h=6.626×10-34J·s。
试计算:
(1)反应的活化能Ea
(2)反应在500K时的活化焓和活化熵
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“双环戊烯单分子气相热分解反应,在483K时的速率常数k(48…”相关的问题
更多“双环戊烯单分子气相热分解反应,在483K时的速率常数k(48…”相关的问题
 2HI+环戊二烯,得到
2HI+环戊二烯,得到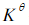 与温度(K)的关系为:
与温度(K)的关系为: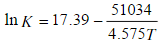
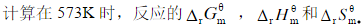
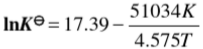 ,试计算:(1)在573K时反应的
,试计算:(1)在573K时反应的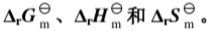 ;(2)若开始时用等物质的量的I2(g)和环戊烯(g)混合,温度为573K,起始总压为101.325kPa,达平衡后I2(g)的分压;(3)起始总压为1013.25kPa,达平衡后I2(g)的分压。
;(2)若开始时用等物质的量的I2(g)和环戊烯(g)混合,温度为573K,起始总压为101.325kPa,达平衡后I2(g)的分压;(3)起始总压为1013.25kPa,达平衡后I2(g)的分压。