 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算OH-浓度为0.100mol·dm-3时,氧的电极电势值。(p(O2)=101.325kPa,T=298.15K)。
计算OH-浓度为0.100mol·dm-3时,氧的电极电势值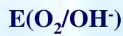 。(p(O2)=101.325kPa,T=298.15K)。
。(p(O2)=101.325kPa,T=298.15K)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算OH-浓度为0.100mol·dm-3时,氧的电极电势值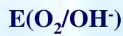 。(p(O2)=101.325kPa,T=298.15K)。
。(p(O2)=101.325kPa,T=298.15K)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“计算OH-浓度为0.100mol·dm-3时,氧的电极电势值…”相关的问题
更多“计算OH-浓度为0.100mol·dm-3时,氧的电极电势值…”相关的问题
将钙离子选择电极与另一参比电极浸入0.100mol·L-1Ca2+标准溶液中,参加电极为负极,于25℃测得电动势为0.250V。用未知溶液代替上述溶液时,测得电动势为0.271V,计算未知液中Ca2+的浓度。
一种氟离子选择性电极对OH的电位选择性系数KP-,OH-=0.10,若试样溶液中的F-浓度为1.5×10-2mol/L时,允许测定误差为5%,问溶液允许的最大pH(以浓度代替活度计算)为多少?
14.某二元酸H2B,已知

反应Zn(s)+Hg2Cl2(s)====2Hg(l)+Zn2+(aq)+2Cl-(aq)在25℃下,当各离子浓度均为1.0mol·dm-3时,测得电池电动势为1.03V,当c(Cl-)=0.100mol·dm-3时,电动势为1.21V,此时c(Zn2+)为多少?
1在烧杯中盛放20.00cm30.100mol·dm-3氨的水溶液,逐步加入0.100mol·dm-3HCl溶液。试计算:

用0.100mol·L-1NaOH溶液滴定0.100mol·L-1HCl和0.20mol·L-1H3BO3混合溶液。若滴定终点比化学计量点时高0.50pH单位,计算终点误差。(H3BO3的Ka=5.8×10-10)
291K时,纯水的电导率κ(H2O)=3.8×10-6S·m-1,当H2O(1)解离成H+和OH-并达到平衡时,求该温度下H2O(1)的摩尔电导率、解离度和H+的浓度。已知这时水的密度为998.6kg·m-3。
A.-0.25℃
B.-0.21℃
C.-0.188℃
D.-0.167℃