 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
光气分解反应COCl2(g)====CO(g)+Cl2(g)在373K时,,试求:
光气分解反应COCl2(g)====CO(g)+Cl2(g)在373K时,K=8.80×10-9求在373K平衡后总压力P总=202.6KPA光气的解离度?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
光气分解反应COCl2(g)====CO(g)+Cl2(g)在373K时,K=8.80×10-9求在373K平衡后总压力P总=202.6KPA光气的解离度?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“光气分解反应COCl2(g)====CO(g)+Cl2(g)…”相关的问题
更多“光气分解反应COCl2(g)====CO(g)+Cl2(g)…”相关的问题
在100℃下,反应COCl2(g)===CO(g)+Cl2(g)的KΘ=8.1×10-9,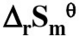 =125.6J·mol-1·K-1。计算:(1)100℃,总压力为200kPa时COCl2的离解度;(2)100℃下上述反应的
=125.6J·mol-1·K-1。计算:(1)100℃,总压力为200kPa时COCl2的离解度;(2)100℃下上述反应的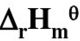 ;(3)总压力为200kPa,COCl2的解离度为0.1%时的温度。设△rCp,m=0。
;(3)总压力为200kPa,COCl2的解离度为0.1%时的温度。设△rCp,m=0。
双光气分解反应ClCOOCCl3(g)→2COCl2(g)为一级反应。将一定量 双光气迅速引入一个280℃的容器中,751s后测得系统压力为2.710kPa;经很长时间反应完了后系统压力为4.008kPa。305℃时重复实验,经320s系统压力为2.838kPa;反应完了后系统压力为3.554kPa。求活化能。
反应① H2O(g),
H2O(g),
② CO(g),
CO(g),
(1)在标准状态下,用C(石墨)还原水制H2(g)和CO(g)的最低温度;
(2)在1073K、100kPa条件下用C(石墨)还原水制H2(g)和CO(g)系统的平衡气相组成为多少?
工业上由CO和H2合成甲醇:CO(g)+2H2====CH3OH(g),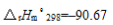 kJ·mol-1,
kJ·mol-1,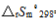 =-221.4J·mol-1·K-1,为了加速反应必须升高温度,但温度又不宜过高。通过计算说明此温度最多不超过多少?
=-221.4J·mol-1·K-1,为了加速反应必须升高温度,但温度又不宜过高。通过计算说明此温度最多不超过多少?
 N2(g)+CO2(g)
N2(g)+CO2(g) <0。欲使有害气体NO、CO尽可能转化为N2和CO2,应采取的条件为:
<0。欲使有害气体NO、CO尽可能转化为N2和CO2,应采取的条件为:A.低温高压;
B.高温高压;
C.低温低压;
D.高温低压。
反应CO(g)+H2O(g)==H2(g)+CO2(g)的标准平衡常数与温度的关系为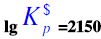 K/T-2.216,当CO、H2O、H2、CO2的起初组成的质量分数分别为0.30、0.30、0.20和0.20,总压为101.3kPa时,在什么温度以下(或以上)反应向生成产物的方向进行?
K/T-2.216,当CO、H2O、H2、CO2的起初组成的质量分数分别为0.30、0.30、0.20和0.20,总压为101.3kPa时,在什么温度以下(或以上)反应向生成产物的方向进行?
已知同一温度,两反应方程及标准平衡常数如下:
(1) C(石墨)+H2O(g)===CO(g)+H2(g)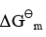
(2) C(石墨)+2H2O(g)===CO2(g)+2H2(g)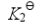
求反应CO(g)+H2O(g)===CO2(g)+H2(g)的KΘ。
已知在温度为298.15K的标准条件下,CO(g)和H2O(g)的标准摩尔生成焓分别为-110.53kJ/mol和-241.83kJ/mol。计算反应H2O(g)+C(石墨)====CO(g)+H2(g)的标准摩尔焓变。
已知298.15K时,CO(g)和CH3OH(g)标准摩尔生成焓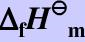 分别为-110.525和-200.66kJ/mol。CO(g)、H2(g)、CH3OH(l)的标准摩尔熵
分别为-110.525和-200.66kJ/mol。CO(g)、H2(g)、CH3OH(l)的标准摩尔熵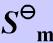 (298.15K)分别为197.67J/(mol·K)、130.68J/(mol·K)及127J/(mol·K)。又知298.15K时甲醇的饱和蒸气压16.59kPa,摩尔气化热
(298.15K)分别为197.67J/(mol·K)、130.68J/(mol·K)及127J/(mol·K)。又知298.15K时甲醇的饱和蒸气压16.59kPa,摩尔气化热 =38.0kJ/mol,蒸气可视为理想气体。利用上述数据,求298.15K时,反应
=38.0kJ/mol,蒸气可视为理想气体。利用上述数据,求298.15K时,反应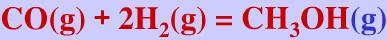 的
的
随温度升高,反应(1):2M(s)+O2(g)=2MO(s)和反应(2):2C(s)+O2(g)=2CO(g)的摩尔吉布斯自由能升高的为______,降低的为______,因此,金属氧化物MO被碳还原反应MO(s)+C(s)=M(s)+CO(g)在高温条件下______向自发。
指出下列各系统的组分数、相数和自由度数各为多少。
(1)NH4Cl(s)在抽空容器中,部分分解为NH3(g)、HCl(g)达平衡;
(2)NH4Cl(s)在含有一定量NH3(g)的容器中,部分分解为NH3(g)、HCl(g)达平衡;
(3)NH4HS(s)与任意量的NH3(g)和H2S(g)混合,达分解平衡;
(4)在900K时,C(s)与CO(g)、CO2(g)、O2(g)达平衡。