 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应的吉布斯自由能ΔG负值越大,则反应的自发性越大,且反应速率也越大。()
反应的吉布斯自由能ΔG负值越大,则反应的自发性越大,且反应速率也越大。( )
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应的吉布斯自由能ΔG负值越大,则反应的自发性越大,且反应速率也越大。( )
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“反应的吉布斯自由能ΔG负值越大,则反应的自发性越大,且反应速…”相关的问题
更多“反应的吉布斯自由能ΔG负值越大,则反应的自发性越大,且反应速…”相关的问题
随温度升高,反应(1):2M(s)+O2(g)=2MO(s)和反应(2):2C(s)+O2(g)=2CO(g)的摩尔吉布斯自由能升高的为______,降低的为______,因此,金属氧化物MO被碳还原反应MO(s)+C(s)=M(s)+CO(g)在高温条件下______向自发。
8.在298.15K时,有下列反应
H3AsO4+2I-+2H+====H3AsO3+I2+H2O
(1) 计算该反应组成的原电池的标准电动势。
(2) 计算该反应的标准摩尔吉布斯自由能变并指出该反应能否自发进行。
(3) 若溶液的的pH=7,而c(H3AsO4)=c(H3AsO3)=c(I-)=1mol·dm-3此反应的△rGm是多少?此时反应进行方向?
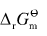 (AgCl)=-109.8kJ·mol-1,则反应2AgCl(s)====2Ag(s)+Cl2(g)的
(AgCl)=-109.8kJ·mol-1,则反应2AgCl(s)====2Ag(s)+Cl2(g)的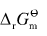 为:
为:A.109.8kJ·mol-1;
B.219.6kJ·mol-1;
C.-109.8kJ·mol-1;
D.-219.6kJ·mol-1。
在常温常压下,HCl(g)的生成热为-92.3kJ·mol-1,生成反应的活化能为113kJ·mol-1,则其逆反应的活化能为______kJ·mol-1。
在一定温度下,将0.5molN2O4(g)放入一密闭容器中,当反应N2O4(g).jpg) 2NO2(g)达到平衡,容器内有0.6molNO2(g),气体总压力为100.0kPa,则该反应的Kθ9为()。
2NO2(g)达到平衡,容器内有0.6molNO2(g),气体总压力为100.0kPa,则该反应的Kθ9为()。
A.0.78
B.1.19
C.0.58
D.1.29
 分别为
分别为 (1)和
(1)和 (2): (1)MnO2(s)====MnO(s)+
(2): (1)MnO2(s)====MnO(s)+ O2(g) (2)MnO2(S)+Mn(s)====2MnO(s) 则298 K时,MnO2(S)的
O2(g) (2)MnO2(S)+Mn(s)====2MnO(s) 则298 K时,MnO2(S)的 等于( )。
等于( )。A.
B.
C.
D.
A.电极极化就是电极的电极电位偏离了由能斯特方程计算出来的平衡电位
B.原电池就是最原始的Cu-Zn电极组成的丹尼尔电池
C.电池的电动势为负值时就是原电池,否则就是电解池
D.可逆电极就是可以进行逆向电化学反应的电极
反应H2(g)+I2(g)→2HI(g)的速率方程为v=k(H2)(I2),能根据这点说它肯定是基元反应______;能否说它肯定是双分子反应______。
A.贝塔系数越大,说明证券的市场风险越大
B.某证券的贝塔系数等于1,则它的风险与整个市场的平均风险相同
C.具有较高贝塔系数的证券不一定就保证有较高的收益
D.大于1的贝塔系数被认为是较高的贝塔值,高贝塔值证券通常被称为进取型证券
E.实际上,贝塔系数为负值的证券不大可能存在
660K时反应2NO(g)+O2(g)====2NO2(g)数据如下表:
| c(NO)/(mol·L-1) | c(O2)/(mol·L-1) | υ/(mol.L-1·s-1) |
| 0.10 0.10 0.20 | 0.10 0.20 0.20 | 0.03 0.06 0.24 |
①写出反应的速率方程;②求反应级数和速率常数;③求C(NO)=c(O2)=0.15mol·L-1时的反应速率。