 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在一封闭容器中混合气体关于压力、体积的下列说法中,()是错误的。A.混合气体中某种气体组分的分压
在一封闭容器中混合气体关于压力、体积的下列说法中,()是错误的。
A.混合气体中某种气体组分的分压力是指某种气体单独占据该容器时具有的压力
B.分体积是指混合气体中某种组分的气体在总压力、温度下所具有的体积
C.混合气体中的某种气体都具有一定的分压力和分体积
D.混合气体中的某种气体的分压力与组分的多少无关
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在一封闭容器中混合气体关于压力、体积的下列说法中,()是错误的。
A.混合气体中某种气体组分的分压力是指某种气体单独占据该容器时具有的压力
B.分体积是指混合气体中某种组分的气体在总压力、温度下所具有的体积
C.混合气体中的某种气体都具有一定的分压力和分体积
D.混合气体中的某种气体的分压力与组分的多少无关
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在一封闭容器中混合气体关于压力、体积的下列说法中,()是错误…”相关的问题
更多“在一封闭容器中混合气体关于压力、体积的下列说法中,()是错误…”相关的问题
A、B两种气体在体积为V的容器中混合,在温度T时测得混合气体的压力为P。若VA、VB分别为两种气体的分体积,PA、PB分别为两种气体的分压力,下列计算式中不正确的一个是
(A) pVA=nART (B) PAVA=nART (C) PAV=nART (D) pA(VA+VB)=nART
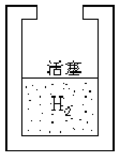
4×10-3kg氢气(看做理想气体)被活塞封闭在某一容器的下半部而与外界平衡(容器开口处有一凸出边缘可防止活塞脱落,如下图所示,活塞的厚度和质量可忽略)。现把2×104J的热量缓慢地传给气体,使气体膨胀。求氢气最后的压强、温度和体积各变为多少?(活塞外大气压处于标准状态下)
1.7. 今有20℃的乙烷-丁烷混合气体,充入一抽成真空的200cm3容器中,直至压力达101.325kPa,测得容器中混合气体的质量为0.3897g。试求该混合气体中两种组分的摩尔分数及分压力。
将装有0.1tool乙醚C2H6OC2H5(1)的小玻璃泡放人35℃、10dm3含氮气的压力为101.325kPa的瓶中,将小泡打碎,乙醚能完全汽化。求 (1)混合气体中乙醚的分压; (2)氮气的△H、△S及△G; (3)乙醚的△H、△S及△G。 已知C2H5OC2H5(1)在101.325kPa时的沸点为35℃,摩尔蒸发焓为25.104 kJ.mol-1。假设容器的体积不变,乙醚蒸气可视为理想气体。
银可能受H2S气体的腐蚀而发生下列反应
H2S(g)+2Ag(s)→Ag2S(s)+H2(g)
已知在298K和100kPa压力下,Ag2S(s)和H2s(g)的标准生成Gibbs自由能 分别为-40.26kJ·mol-1和-33.02kJ·mol-1。试问在298K和100kPa压力下,
分别为-40.26kJ·mol-1和-33.02kJ·mol-1。试问在298K和100kPa压力下,
(1)在H2S(g)和H2(g)的等体积的混合气体中,Ag是否会被腐蚀生成Ag2S(s)?
(2)在H2S(g)和H2(g)的混合气体中,H2S(g)的摩尔分数低于多少时便不至于使Ag被腐蚀?
373K时,在1.0dm3容器中装入0.02mol的苯蒸气和0.02mol水蒸气的混合气体。在恒温条件下把混合气体压缩为原体积的一半,求混合气体的总压。(已知在373K时苯的饱和蒸气压为1.74×105Pa)
一容器中装有某气体1.2dm3,在97.272kPa下,气体从环境吸热800J后,体积膨胀到1.5dm3,计算系统的热力学能改变量。
1.jpg)
Ag受到H2S的腐蚀而可能发生下面的反应: H2S(g)+2Ag(s)
 Ag2S(s)+H2(g) 今在298K、100kPa下,将Ag放在由等体积的H2和H2S组成的混合气中,试问:(1)是否可能发生腐蚀而生成Ag2S;(2)在混合气体中,H2S的百分数低于多少,才不致发生腐蚀。已知298K时,Ag2S和H2S的标准摩尔生成吉布斯函数分别为:一40.25kJ/mol和一32.93kJ/mol。
Ag2S(s)+H2(g) 今在298K、100kPa下,将Ag放在由等体积的H2和H2S组成的混合气中,试问:(1)是否可能发生腐蚀而生成Ag2S;(2)在混合气体中,H2S的百分数低于多少,才不致发生腐蚀。已知298K时,Ag2S和H2S的标准摩尔生成吉布斯函数分别为:一40.25kJ/mol和一32.93kJ/mol。
在一定温度下,将0.5molN2O4(g)放入一密闭容器中,当反应N2O4(g).jpg) 2NO2(g)达到平衡,容器内有0.6molNO2(g),气体总压力为100.0kPa,则该反应的Kθ9为()。
2NO2(g)达到平衡,容器内有0.6molNO2(g),气体总压力为100.0kPa,则该反应的Kθ9为()。
A.0.78
B.1.19
C.0.58
D.1.29
在一逆流吸收塔中,用清水吸收混合气体中的CO2。惰性气体处理量为300m3/h,进塔气体中含CO28%(体积分数),要求吸收率95%,操作条件下摩尔比关系为Y*=1600X,操作液气比为最小液气比的1.5倍。
求: