 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
取家用漂白液试液25.00mL,移入250mL容量瓶中,加水至刻度后,吸取50.00mL,加入碘化钾,加酸酸化后析出碘,用0.0
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“取家用漂白液试液25.00mL,移入250mL容量瓶中,加水…”相关的问题
更多“取家用漂白液试液25.00mL,移入250mL容量瓶中,加水…”相关的问题
用氟离子选择性电极测定牙膏中F-含量。称取0.2000g牙膏并加入50mL缓冲试剂,搅拌微沸冷却后移入100mL容量瓶中,用蒸馏水稀释至刻度。移取25.00mL于烧杯中测得其电位值为0.155V,加入0.10mL0.50mg·mL-1F标准溶液后,测得电位值为0.134V。该离子选择电极的斜率为59.0mV/pF。试计算牙膏中氟的质量分数。
为测定HCl与H3PO4混合溶液中各钼分的浓度,取两份此试液。每份25.00mL,分别用0.2500mol·L-1NaOH标准溶液滴定,第一份用甲基橙为指示剂,消耗30.00mLNaOH标准溶液,第二份用酚酞为指示剂,消耗40.00mL。溶液中HCl与H3PO4的浓度关系是
A.C(H3P04)=c(HCl) B.c(H3PO4)=2c(HCl)
C.2c(H3PO4)=c(HCl)
移取25.00mLHCOOH和HAc的混合溶液,以酚酞为指示剂,用0.1000mol·L-1NaOH滴定至终点,消耗35.20mL。另取25.00mL混合试液,调节为强碱性,加入50.00mL0.01500mol·L-1KMnO4溶液将HCOOH氧化至CO2。酸化溶液,加入0.1000mol·L-1Fe2+溶液25.00mL,然后再用上述KMnO4溶液滴定,用去32.00mL,计算混合液中HCOOH和HAc的浓度各为多少?
移取20.00mL HCOOH和HAc的混合溶液,以0.1000mol·L-1NaOH溶液滴定至终点时,共消耗25.00mL。另取上述溶液20.00mL,准确加入0.02500mol·L-1KMnO4强碱性溶液50.00mL,使其反应完全后,调至酸性,加入0.20000mol·L-1Fe2+标准溶液40.00mL,将剩余的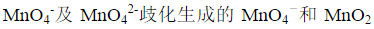 全部还原至Mn2+,剩余的Fe2+溶液用上述KMnO4标准溶液滴定,至终点时消耗24.00mL。计算试液中HCOOH和HAc的浓度。
全部还原至Mn2+,剩余的Fe2+溶液用上述KMnO4标准溶液滴定,至终点时消耗24.00mL。计算试液中HCOOH和HAc的浓度。
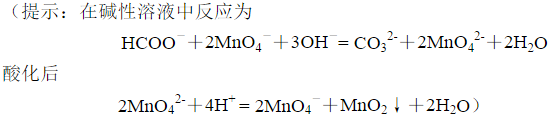
以分光光度法测某电镀废水中的铬(Ⅵ)。取500mL水样,经浓缩和预处理后转入100mL容量瓶中定容,取出20mL试液,调整酸度,加入二苯碳酰二肼溶液显色,定容为25.00mL,以5.0cm吸收池于540nm波长下测得吸光度为0.540。求铬(Ⅵ)的质量浓度ρ(mg·L-1)。已知ε540=4.2×104L·mol-1·cm-1,M(Cr)=52.00g·mol-1。
样试液,分别放入两个50.00mL容量瓶中,其中一个再加入10.00mL(20.0mg·L-1)标准钼溶液,都稀释到刻度。在原子吸收分光光度计上分别测得吸光度为0.314和0.586。计算矿石中钼的质量分数。
25℃时,用氟离子选择性电极测定水样中的氟。取水样25.00mL,加TISAB溶液25mL,测得氟电极相对于SCE的电势(即工作电池的电动势)为+0.1372V;再加入1.00×10-3mol·L-1标准氟溶液1.00mL,测得其电势值为+0.1170V(相对于SCE)。忽略稀释影响,计算水样中氟离子的浓度。
入Cd标准溶液[ρ(Cd)=10μg/ml],用纯水稀释至刻度。用AAS法测得结果见表,计算试样中Cd的含量(μg/g)。
| AAS标准加入法测定Cd结果 | |||
| 序号 | 试液体积(ml) | 加入Cd标液体积(ml) | 吸光度 |
| 0 1 2 3 4 | 10.00 10.00 10.00 10.00 10.00 | 0 1 2 3 4 | 0.042 0.080 0.116 0.153 0.190 |
某水溶液中含有HCl与H2CrO4,吸取25.00mL试液,用0.2000mol·L-1NaOH滴定剂滴至百里酚酞指示剂变色时,消耗40.00mL。另取25.00mL试液,加入过量KI和酸,使之析出碘,用0.1000mol·L-1Na2S2O3滴定至终点时,消耗40.00mL。计算在25.00mL试样中含HCl、H2CrO4各多少克?HC[与H2CrO4的浓度各为多少?
液,以EDTA滴定,用去0.02043m01·L-1EDTA溶液17.50mL,求该石灰石中CaO的质量分数。
某未知Ni2+试液,直流极谱法测得其波高为4.80mm(剩余电流已扣除)。加入0.50mL 1.00×10-3mol·L-1Ni2+标准溶液于25.00mL未知Ni2+试液中,测得其波高为7.20mm。计算该未知液中Ni2+的浓度。