 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知2N2O====4NO2+O2,反应机理如下: N2O====NO2+NO3(快) NO2+NO3====NO+O2+NO2(慢) NO+NO3====2NO2(快)
已知2N2O====4NO2+O2,反应机理如下:
N2O====NO2+NO3(快)
NO2+NO3====NO+O2+NO2(慢)
NO+NO3====2NO2(快)
该反应速率方程为______,它是一个______级反应
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知2N2O====4NO2+O2,反应机理如下:
N2O====NO2+NO3(快)
NO2+NO3====NO+O2+NO2(慢)
NO+NO3====2NO2(快)
该反应速率方程为______,它是一个______级反应
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知2N2O====4NO2+O2,反应机理如下: N2O=…”相关的问题
更多“已知2N2O====4NO2+O2,反应机理如下: N2O=…”相关的问题
已知298.15K时,电极反应: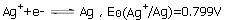 ,Ag2C2O4的Ksp为3.5×10-11,求电极反应Ag2C2O2+2e-
,Ag2C2O4的Ksp为3.5×10-11,求电极反应Ag2C2O2+2e- 2Ag+C2O2-4的标准电极电势
2Ag+C2O2-4的标准电极电势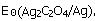 。
。
已知电极反应Cu2++2e====Cu的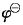 为0.34V,则电极反应:2Cu-4e====2Cu2+的
为0.34V,则电极反应:2Cu-4e====2Cu2+的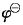 值为( )。
值为( )。
(A) -0.68V (B) +0.68V (C) -0.34V (D) 0.34V
10.已知

的标准电极电势以及当
已知298.15K时, ,
, ,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的
,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的 ;(4)计算电池反应的
;(4)计算电池反应的 ;(5)求AgI的Ksp。
;(5)求AgI的Ksp。
在间歇搅拌釜式反应器中进行等温一级反应,A→R+S,已知:反应达30s时,A的转化率为90%,试求转化率达99%时还需要多少时间?
已知醋酸可的松半衰期为100min,反应200min后,残存率是
A.90%.
B.80%.
C.75%.
D.50%.
E.25%.
甲烷在1bar,700℃时反应生成炭黑,计算平衡气相转化率,以及反应后纯甲烷的摩尔分数。已知温度为700℃时,Ka=7.403,反应中甲烷和氢气为气体,炭黑为固体。
已知常压下,20℃时,CO2在水中的亨利系数为1.44×105kPa,并且已知以下两个反应的平衡常数
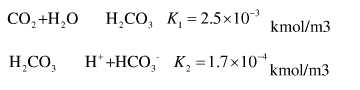
若平衡状态下气相中的CO2分压为10kPa,求水中溶解的CO2的浓度。
(CO2在水中的一级解离常数为K=4.3×10-7kmol/m3,实际上包含了上述两个反应平衡,K=K1K2)
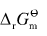 (AgCl)=-109.8kJ·mol-1,则反应2AgCl(s)====2Ag(s)+Cl2(g)的
(AgCl)=-109.8kJ·mol-1,则反应2AgCl(s)====2Ag(s)+Cl2(g)的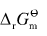 为:
为:A.109.8kJ·mol-1;
B.219.6kJ·mol-1;
C.-109.8kJ·mol-1;
D.-219.6kJ·mol-1。