 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
一高压容器中含有未知气体,可能是N2或Ar.在298 K时取出试样,从5×10-3m3绝热膨胀到6×10-3m3,温度
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“一高压容器中含有未知气体,可能是N2或Ar.在298 K时取…”相关的问题
更多“一高压容器中含有未知气体,可能是N2或Ar.在298 K时取…”相关的问题
一个体积为V的导热容器被不可穿透的隔板分成左右两部分,体积分别为V1和V2,内部充满稀薄气体.令容器置于温度为T的热库之中,系统与热库交换热量达热平衡.假定温度较高,气体可视为理想气体.
(1)左边气体由N1个He4分于构成,石边气体由N2个He3分于构成,在隔板上开一小孔,使两边的气体可均匀混合,试求开孔前后气体熵的改变;
(2)两边均为He4气体,试求开孔前后气体熵的改变.
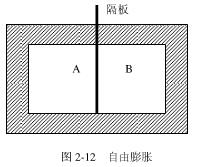
气的热力学能将如何变化?若在隔板上有一小孔,气体泄漏入B中,分析A、B两部分压力相同时,A、B两部分气体热力学能如何变化?
 N2(g)+CO2(g)
N2(g)+CO2(g) <0。欲使有害气体NO、CO尽可能转化为N2和CO2,应采取的条件为:
<0。欲使有害气体NO、CO尽可能转化为N2和CO2,应采取的条件为:A.低温高压;
B.高温高压;
C.低温低压;
D.高温低压。
容器中放有100g N2,温度与压力分别为25℃和3039.75kPa,若该气体反抗1013.25kPa压力等外压绝热膨胀,试计算系统的最终温度T和过程的△U、△H。假定N2是理想气体,且CV,m=20.71J·mol-1·K-1。
有两台机器生产金属部件.分别在两台机器所生产的部件中各取一容量n1=60,n2=40的样本,测得部件重量(以kg计)的样本方差分别为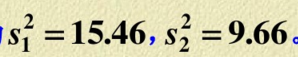 .设两样本相互独立.两总体分别服从
.设两样本相互独立.两总体分别服从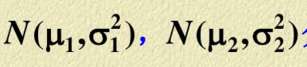 分布.
分布.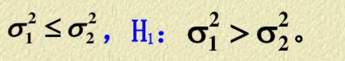 均未知.试在显著性水平α=0.05下检验假设
均未知.试在显著性水平α=0.05下检验假设
已知反应2SO2+O2====2SO3在1062K时的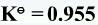 ,如果在该温度下,于某一容器中含有SO2,O2,SO3三种气体,其分压力分别为:p(SO2)=30.4kPa,P(O2)=60.1kPa,P(SO3)=25.3kPa。试判断反应进行的方向。
,如果在该温度下,于某一容器中含有SO2,O2,SO3三种气体,其分压力分别为:p(SO2)=30.4kPa,P(O2)=60.1kPa,P(SO3)=25.3kPa。试判断反应进行的方向。
一容积为V=1.0m3的容器内装有N1=1.0×1024个氧分子和N2=3.0×1024个氮分子的混合气体,混合气体的压强p=2.58×104Pa。试求:

统所能达到的最高温度和最大压力。空气组成按y(O2,g)=0.21,y(N2,g)=0.79计算。水蒸气的标准摩尔生成焓见附录(在教材中)。各气体的平均摩尔定容热容分别为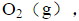
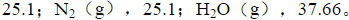 假设气体适用于理想气体状态方程。
假设气体适用于理想气体状态方程。
1molH2与过量50%空气混合物的始态为25℃、101.325kPa。若该混合气体于容器中发生爆炸,试求所能达到的最高爆炸温度与压力。设所有气体均可按理想气体处理。H2O(g)、O2及N2的平均定容摩尔热容分别为37.66J·mol-1·K-1、25.1J·mol-1·K-1及25.1J·mol-1·K-1。