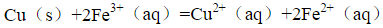更多“计算体系的标准电极电势。 (已知[Ag(NH3)2]+的K稳…”相关的问题
更多“计算体系的标准电极电势。 (已知[Ag(NH3)2]+的K稳…”相关的问题
10.已知

的标准电极电势以及当
已知电对Ag+/Ag的标准电极电势喂0.799V,Agcl的Kf=1.6×107,试求新电对AgCl/Ag的标准电极电势。
已知298.15K时,电极反应: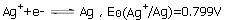 ,Ag2C2O4的Ksp为3.5×10-11,求电极反应Ag2C2O2+2e-
,Ag2C2O4的Ksp为3.5×10-11,求电极反应Ag2C2O2+2e- 2Ag+C2O2-4的标准电极电势
2Ag+C2O2-4的标准电极电势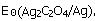 。
。
已知电池(-)Cu|Cu2+(0.1mol·dm-3)||Ag+(0.01mol·dm-3)|Ag(),

计算25℃时,下列电池的电动势,并标明电池的正负极。
已知:E(AgCl/Ag)=0.222V,φSCE=0.245V
Ag,AgCl|NaCl(0.1mol·L-1),NaF(0.001mol·L-1)|LaF3单晶膜|NaF(0.1nol·L-1)‖SCE
电解时,在阳极上首先发生氧化作用而放电的是( )。
(A) 标准还原电极电势最大者
(B) 标准还原电极电势最小者
(C) 考虑极化后,实际还原电极电势最大者
(D) 考虑极化后,实际还原电极电势最小者
9.电解时,在阳极上首先发生氧化作用而放电的是( )。
(A) 标准还原电极电势最大者
(B) 标准还原电极电势最小者
(C) 考虑极化后,实际还原电极电势最大者
(D) 考虑极化后,实际还原电极电势最小者
求1.0L 1.0mol·L-1Na2S2O3溶液能溶解多少克AgBr?
(已知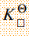 [Ag(S2O3)2]3-=2.4×1013,
[Ag(S2O3)2]3-=2.4×1013,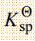 (AgBr)=5.0×10-13,AgBr相对分子质量187.8)
(AgBr)=5.0×10-13,AgBr相对分子质量187.8)
已知298.15K时, ,
, ,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的
,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的 ;(4)计算电池反应的
;(4)计算电池反应的 ;(5)求AgI的Ksp。
;(5)求AgI的Ksp。

![计算体系的标准电极电势。 (已知[Ag(NH3)2]+的K稳=1.7×107,](https://img2.soutiyun.com/ask/uploadfile/6018001-6021000/39ef16c84c721c57e1a00d2921800d9c.jpg)

 如果结果不匹配,请
如果结果不匹配,请