 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
理想气体反应N2O5(g)===N2O4(g)+(1/2)O2(g)的 为41.84kJ·mol-1,△Cp,m=0。要增加N2O4的产率可以:( )。
为41.84kJ·mol-1,△Cp,m=0。要增加N2O4的产率可以:( )。
A.降低温度
B.提高温度
C.提高压力
D.等温等容加入惰性气体
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 为41.84kJ·mol-1,△Cp,m=0。要增加N2O4的产率可以:( )。
为41.84kJ·mol-1,△Cp,m=0。要增加N2O4的产率可以:( )。A.降低温度
B.提高温度
C.提高压力
D.等温等容加入惰性气体
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“理想气体反应N2O5(g)===N2O4(g)+(1/2)O…”相关的问题
更多“理想气体反应N2O5(g)===N2O4(g)+(1/2)O…”相关的问题
在一定温度下,将0.5molN2O4(g)放入一密闭容器中,当反应N2O4(g).jpg) 2NO2(g)达到平衡,容器内有0.6molNO2(g),气体总压力为100.0kPa,则该反应的Kθ9为()。
2NO2(g)达到平衡,容器内有0.6molNO2(g),气体总压力为100.0kPa,则该反应的Kθ9为()。
A.0.78
B.1.19
C.0.58
D.1.29
反应A(g)+B(s)→C(g),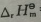 =-41.8kJ·mol-1,A、C都是理想气体。在25℃和标准压力下,按下列过程发生变化:体系做了最大功,放热1.67kJ·mol-1。则此变化过程Q=______,W=______,
=-41.8kJ·mol-1,A、C都是理想气体。在25℃和标准压力下,按下列过程发生变化:体系做了最大功,放热1.67kJ·mol-1。则此变化过程Q=______,W=______,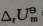 =______,
=______,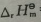 =______ 。
=______ 。
由A-B组成的二元汽液平衡系统,若汽相为理想气体,液相活度系数模型符合对称归一化条件,其超额Gibbs函数符合GE/RT=βxAxB,β是温度的函数,测得80℃时二组分的无限稀释活度系数是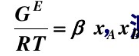 ,两纯组分的蒸气压为
,两纯组分的蒸气压为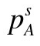 =120kPa,
=120kPa,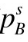 =80kPa,试问该系统在80℃时是否存在共沸点?若有,计算共沸点组成和压力。
=80kPa,试问该系统在80℃时是否存在共沸点?若有,计算共沸点组成和压力。
在一个带活塞(无摩擦无质量)的容器中,有氮气0.5mol,容器底部有一个密闭小瓶,瓶中有水1.5mol。系统温度保持373.2K、101.325kPa,使小瓶破碎,在维持压力为101.325kPa下水蒸发为水蒸气,终态温度仍为373.2K。求此过程中的Q、W、△U、△H、△S、△G、△F。已知水在373.2K、101.325kPa下的摩尔蒸发热为40.67kJ/mol,氮气和水蒸气均按理想气体处理。
反应H2(g)+I2(g)→2HI(g)的速率方程为v=k(H2)(I2),能根据这点说它肯定是基元反应______;能否说它肯定是双分子反应______。
已知反应:mA(g)+nB(g)=pC(g)+qD(g),当压缩体积使体系总压力增大一倍时,该反应的反应速率增大到原来的4倍,则(m+n)等于( )。
(A) 1 (B) 2 (C) 4 (D) 0
对于基元反应2NO(g)+O2(g)====2NO2(g),一定温度下,若反应器体积缩小一半,则正反应速率是原来的______倍。
氢气和氯气化合形成氯化氢的反应:H2(g)+Cl2(g)→2HCl(g),根据下列反应机制推导其速率方程:
(1) (快速平衡)
(快速平衡)
(2)Cl+H2→HCl+H (慢)
(3)H+Cl2→HCl+Cl (快)
试求1000K时,反应的标准摩尔反应焓。。CH3COOH(g)、CH4(g)、CO2(g)的平均定压摩尔热容Cp,m别为52.3J·mol-1·K-1、31.4J·mol-1·K-1及37.7J·mol-1·K-1。
