 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
由两个氢半电池Pt,H2(φΘ)丨 H+(0.1molL-1)和Pt,H2(pΘ)丨H+(xmolL-1)组成一原电池,测得该原电池的
由两个氢半电池Pt,H2(φΘ)丨 H+(0.1molL-1)和Pt,H2(pΘ)丨H+(xmolL-1)组成一原电池,测得该原电池的电动势为0.016V,若pt,H2(pΘ)丨H+(xmolL-1)作为原电池的正极,问组成该半电池的溶液中H+浓度是多少?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
由两个氢半电池Pt,H2(φΘ)丨 H+(0.1molL-1)和Pt,H2(pΘ)丨H+(xmolL-1)组成一原电池,测得该原电池的电动势为0.016V,若pt,H2(pΘ)丨H+(xmolL-1)作为原电池的正极,问组成该半电池的溶液中H+浓度是多少?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“由两个氢半电池Pt,H2(φΘ)丨 H+(0.1molL-1…”相关的问题
更多“由两个氢半电池Pt,H2(φΘ)丨 H+(0.1molL-1…”相关的问题
原电池的电池符号为: (-)Pt,H2(100kPa)丨H+(1.0molL-1) ‖ c12(100kPa)丨 Cl-(1.0molL-1)丨 Pt()
写出电极反应及电池反应;
由两个氢电极Pt|H2(100kPa)|H+(0.10mol·dm-3)和Pt|H2(100kPa)|H+(xmol·dm-3)组成的原电池,测得该原电池的电动势为0.016V。若后一电极作为该原电池的正极,问组成该电极的溶液中的H+的浓度x值为多少?
由两个氢电极H2(100kPa)|H+(0.10mol·dm-3)|Pt和H2(100kPa)|H+(xmol·dm-3)|Pt组成原电池,测得该原电池的电动势为0.016V。若后一电极作为该原电池的正极,求组成该电极的溶液中H+的浓度x的值。
有一电池(-)Pt,H2(50kPa)|H+(0.50mol·L-1)||Sn4+(0.70mol·L-1),Sn2+(0.50mol·L-1)|Pt()
(1)写出半反应
(2)写出电池反应
(3)计算原电池的电动势E
(4)当E=0时,在保持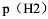 和
和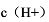 不变的情况下,
不变的情况下,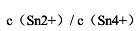 等于多少?
等于多少?
根据以下两个电池求出胃液的pH。
(1)(—)Pt|H2(100kPa)|H+(1.0mol·L-1)||KCl(0.1mol·L-1)|Hg2Cl2(s),Hg()
25℃时测得E=+0.3338V。
(2)(—)Pt|H2(100kPa)|胃液||KCl(0.1mol·L-1)|Hg2Cl2(s),Hg()
25℃时测得E=+0.420V。
有一原电池,其电池符号为Pt,H2(50kPa)|H+(0.50mol·dm-3)||Sn4+(0.70mol·dm-3),Sn2+(0.50mol·dm-3)|Pt

根据标准电极电势计算298 K时下列电池的电动势及电池反应的平衡常数。
(1)(-)Pb|Pb2+(0.1mol·L-1)||Cu2+(0.5mol·L-1)|Cu()
(2)(-)Sn|Sn2+(0.05mol·L-1)||H+(1.0mol·L-1)|H2(105Pa)|Pt()
(3)(-)Pt|H2(105Pa)|H+(1mol·L-1)||Sn4+(0.5mol·L-1),Sn2+(0.1mol·L-1)|Pt()
(4)(-)Pt|H2(105Pa)|H+(0.01mol·L-1)||H+(1.0mol·L-1)|H2(105Pa)|Pt()
有一电池: (一)Pt,H
A.Pt|H2|H+(aq)||OH-(aq)|O2|Pt
B.Pt|H2|NaOH(aq)|O2|Pt
C.Pt|H2|NaOH(aq)||HCl(aq)|H2|Pt
D.Pt|H2(p1)|H2O(l)|H2(p2)|Pt
19,有电池Pt|H2(




 H+(
H+(

