 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
应用德拜-休克尔公式计算25℃时下列各溶液中的γ±: (1)0.005mol·kg-1NaBr;(2)0.001mol·kg-1ZnSO4。
应用德拜-休克尔公式计算25℃时下列各溶液中的γ±:
(1)0.005mol·kg-1NaBr;(2)0.001mol·kg-1ZnSO4。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
应用德拜-休克尔公式计算25℃时下列各溶液中的γ±:
(1)0.005mol·kg-1NaBr;(2)0.001mol·kg-1ZnSO4。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“应用德拜-休克尔公式计算25℃时下列各溶液中的γ±: (1)…”相关的问题
更多“应用德拜-休克尔公式计算25℃时下列各溶液中的γ±: (1)…”相关的问题
写出下列各电池的电池反应。应用表7.7.1(在教材中)的数据计算25℃时各电池的电动势及电池反应的摩尔吉布斯函数变,并指明各电池反应能否自发进行。
(1)Pt|H2(g,100kPa)|HCl[a(HCl)=1]|Cl2(g,100kPa)|Pt
(2)Zn|ZnCl2[a(ZnCl2)=0.5]|AgCl(S)|Ag
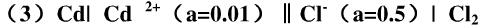
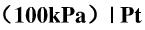
在25℃时用下列电池
标准氢电极|待测pH试液||饱和甘汞电极测得如下一系列溶液的电动势,试根据电动势计算溶液的pH。
当下列电池中的标准溶液是pH=5.21的缓冲溶液时,在25℃时的电动势为0.209V。
玻璃电极|H+(a)||SCE。
当缓冲溶液由待测试液代替时,测得的电动势为0.312V,计算待测试液的pH。
计算一维环形原子链(原子质量m、弹性系数K、原子数N)的摩尔热容:
(1) 用德拜模型;
(2) 用精确的态密度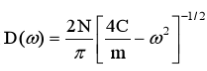 ;
;
(3) 对固定的原子质量m、弹性系数K,(1)和(2)中哪个计算出来的比热容比较大?用低温展开证明你的观点。
应用附录(在教材中)中有关物质热化学的数据,计算25℃时反应
2CH3OH(1)+O2(g)===HCOOCH3(1)+2H2O(1)的标准摩尔反应焓,
要求:
(1)应用25℃的标准摩尔生成焓的数据:△fHmΘ(HCOOCH3,1)=-379.07kJ·mol-1;
(2)应用25℃的标准摩尔燃烧焓的数据。
pH玻璃电极与饱和甘汞电极组成如下电池:玻璃电极|H+(x)‖饱和甘汞电极。测定pH为4.01的邻苯二甲酸氢钾缓冲溶液时,其电池电动势为0.211V。而测定两个未知溶液时,其电池电动势分别为0.435V和0.0186V,试计算两种未知溶液的pH(25℃)。
A.本期资产增加=(本期销售增加/基期销售收入)×基期期末总资产
B.本期负债增加=基期销售收入×销售净利率×利润留存率×(基期期末负债/基期期末股东权益)
C.本期股东权益增加=基期销售收入×销售净利率×利润留存率
D.本期销售增加=基期销售收入×(基期净利润/基期期初股东权益)×利润留存率
根据对现金流量的理解,则计算营业现金流量时,每年净现金流量可按下列公式()来计算。
A.净现金流量=每年营业收入一付现成本
B.净现金流量=每年营业收入一付现成本一所得税
C.净现金流量=净利+折旧+所得税
D.净现金流量=净利+折旧一所得税