 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在25℃时用下列电池 标准氢电极|待测pH试液||饱和甘汞电极测得如下一系列溶液的电动势,试根据电动势计算溶
在25℃时用下列电池
标准氢电极|待测pH试液||饱和甘汞电极测得如下一系列溶液的电动势,试根据电动势计算溶液的pH。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在25℃时用下列电池
标准氢电极|待测pH试液||饱和甘汞电极测得如下一系列溶液的电动势,试根据电动势计算溶液的pH。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在25℃时用下列电池 标准氢电极|待测pH试液||饱和甘汞电…”相关的问题
更多“在25℃时用下列电池 标准氢电极|待测pH试液||饱和甘汞电…”相关的问题
用标准甘汞电极作正极,氢电极作负极(pH2=100kPa)与待测的HCl溶液组成电池。在25℃时,测得E=0.342V。当待测溶液为NaOH溶液时,测得E=1.050V。取此NaOH溶液20.00mL,用上述HCl溶液中和完全,需用HCl溶液多少毫升?
25℃时,用钙离子选择性电极(负极)与饱和甘汞电极(正极)组成电池,在25.0mL试液中测得电动势为0.4965V,加入2.00mL 5.45×10-2mol·L-1Ca2+标准溶液后,测得电动势为0.4117V,试求试液的p(Ca2+)。
25℃时,用pH=4.00的标准缓冲溶液,测得电池:“玻璃电极|H+(a=Xmol·L-1)‖饱和甘汞电极”的电动势为0.814V,那么在c(HAc)=1.00×10-3mol·L-1的醋酸溶液中,此电池的电动势为多少?(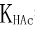 =1.8×10-5,设a(H+)=[H+])
=1.8×10-5,设a(H+)=[H+])
当下列电池中的标准溶液是pH=5.21的缓冲溶液时,在25℃时的电动势为0.209V。
玻璃电极|H+(a)||SCE。
当缓冲溶液由待测试液代替时,测得的电动势为0.312V,计算待测试液的pH。
A.待测离子到达电极表面的速率;
B.电池电动势的数值;
C.电极膜的厚度,表面光洁度;
D.介质的离子强度。
pH玻璃电极与饱和甘汞电极组成如下电池:玻璃电极|H+(x)‖饱和甘汞电极。测定pH为4.01的邻苯二甲酸氢钾缓冲溶液时,其电池电动势为0.211V。而测定两个未知溶液时,其电池电动势分别为0.435V和0.0186V,试计算两种未知溶液的pH(25℃)。
准确量取30.00 mL弱酸HA,加水稀释至100.00 mL,在电池:(—)SHE|HA || SCE()中,以0.100 0 mol·L-1NaOH标准溶液滴定之。25℃时,当弱酸HA被中和一半时,电池电动势为0.524 V,化学计量点时,电池电动势为0.749 V。求:(1)弱酸HA的电离常数Kα值。(2)原弱酸HA溶液的浓度?(已知饱和甘汞电极的电极电位为0.244 V)
将下列反应组成原电池(温度为298.15K):2Fe3++Cu====2Fe2++Cu2+
(1)计算原电池的标准电动势;(2)写出其电池符号;(3)指出正极、负极,并写出电极反应;(4)当Cu2+的浓度升到10mol·L-1时,原电池的电动势为多少?