 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
乙醛在密闭容器中按CH3CHO(g)→CH4(g)+CO(g)分解。在518℃,乙醛起始压力为48.4 kPa,不断测定容器内
乙醛在密闭容器中按CH3CHO(g)→CH4(g)+CO(g)分解。在518℃,乙醛起始压力为48.4 kPa,不断测定容器内的总压力,其变化情况如下表所示:
 试证明它是二级反应,并计算速率常数。
试证明它是二级反应,并计算速率常数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
乙醛在密闭容器中按CH3CHO(g)→CH4(g)+CO(g)分解。在518℃,乙醛起始压力为48.4 kPa,不断测定容器内的总压力,其变化情况如下表所示:
 试证明它是二级反应,并计算速率常数。
试证明它是二级反应,并计算速率常数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“乙醛在密闭容器中按CH3CHO(g)→CH4(g)+CO(g…”相关的问题
更多“乙醛在密闭容器中按CH3CHO(g)→CH4(g)+CO(g…”相关的问题
气态乙醛在518℃时的热分解反应如下 CH3CHo(g)→CH4(g)+C0(g) 此反应在密闭容器中进行,初始压力为48.39kPa,压力增加值与时间的关系如下
1.jpg) 试求反应级数和速率系数(浓度以mol.dm-3为单位,时间以s为单位)。
试求反应级数和速率系数(浓度以mol.dm-3为单位,时间以s为单位)。
气态乙醛在791K时的热分解反应为:
CH3CHO→CH4+CO
在密闭真空容器中进行,充以初压为48.4kPa的气态乙醛,发生上述分解反应,已知压力增加值Δp与时间t的关系数据如下:求写出反应速率和有关化学方程式?
| t/s | 42.0 | 105 | 242 | 840 | 1440 |
| Δp/kPa | 4.53 | 9.86 | 17.86 | 32.53 | 37.86 |
PCl5遇热按PCl5(g)=PCl3(g)+Cl2(g)式分解。2.695g PCl5装在1.00 dm3的密闭容器中,求在523 K时: (1)当总压力1000 kPa时,PCl5的分解率是多少? (2)要使分解率低于10%,总压力是多少?
统所能达到的最高温度和最大压力。空气组成按y(O2,g)=0.21,y(N2,g)=0.79计算。水蒸气的标准摩尔生成焓见附录(在教材中)。各气体的平均摩尔定容热容分别为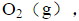
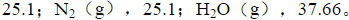 假设气体适用于理想气体状态方程。
假设气体适用于理想气体状态方程。
在一定温度下,将0.5molN2O4(g)放入一密闭容器中,当反应N2O4(g).jpg) 2NO2(g)达到平衡,容器内有0.6molNO2(g),气体总压力为100.0kPa,则该反应的Kθ9为()。
2NO2(g)达到平衡,容器内有0.6molNO2(g),气体总压力为100.0kPa,则该反应的Kθ9为()。
A.0.78
B.1.19
C.0.58
D.1.29
A.向右移动
B.向左移动
C.不移动
D.无法确定
设有一反应2A(g)+B(g)→G(g)+H(s)在某恒温密闭容器中进行,开始时A和B的物质的量之比为2:1,起始总压为3.0kPa,在400K时,60s后容器中的总压力为2.0kPa,设该反应的速率方程为
变分子反应的计算比较
乙醛分解反应,反应式为
CH3CHO→CH4+CO
乙醛在520℃和0.1MPa大气压下以0.1kg/s流率进入理想管式反应器进行分解反应。已知在该反应条件下反应为不可逆二级反应,反应速率常数k=0.43×10-3m3/(mol·s)=0.43m3/(kmol·s)。试求进料乙醛分解35%的反应容积、空时和平均停留时间。
在523.15K时,将0.70molPCl5(g)置于2.0L密闭容器中,待其达到平衡
PCl5(g) PCl3(g)+Cl2(g)经测定PCl5(g)的物质的量为0.20mol。
PCl3(g)+Cl2(g)经测定PCl5(g)的物质的量为0.20mol。
(1)求该反应的标准平衡常数KΘ及PCl5(g)的平衡转化率α。
(2)在上述平衡系统中再加入0.10mol PCl5(g),求重新达平衡后各物质的平衡分压。
在375K时反应SO2Cl2(g)=SO2(g)+Cl2(g)的标准平衡常数Kθ为2.4。今将5.4g的SO2Cl2(g)置于密闭容器中,并加热到375K。(1) 假定SO2Cl2(g)不解离,它的压力将是多少?(2) 平衡时SO2Cl2(g)、SO2(g)和Cl2(g)的分压各是多少?
25℃下,密闭恒容的容器中有10g固体萘(C10H8,s)在过量的O2(g)中完全燃烧成CO2(g)和H2O(1)。若过程放热401.727kJ,求:
(1)c10H8(s)+12O2(g)===10CO2(g)+4H2O(1)的反应进度;(2)C10H8(s)的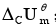 (3)C10H8(s)的
(3)C10H8(s)的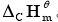 。
。